Введение
Развитие, прогноз, способы лечения и профилактики келоидных рубцов представляют сложную и актуальную медико-социальную проблему. Патогенез келоидных рубцов не установлен.
В связи с отсутствием единого подхода к определению критериев эффективности лечения вопрос о тактике лечения данной нозологии остается дискуссионным. Это связано с недостаточной эффективностью традиционно используемых методов лечения (хирургическое иссечение, гормоно-, рентгено-, ферментотерапия, криодеструкция, СВЧ-криодеструкция), после применения которых рецидивы возникают в 30–50% случаев, а косметический результат зачастую не оправдывает ожиданий [8]. Поиски новых методов лечения и профилактики, которые приостановили бы прогрессирование келоида и его рецидива, не прекращаются до сих пор [6, 8].
В последние годы появились многочисленные исследования, в которых рекомендуется использовать антигомотоксические лекарственные средства при травмах и после хирургических вмешательств [3]. Терапевтический подход к гомотоксикологии аналогичен общепринятой терапии: диагностика и назначение комплексных биологических препаратов осуществляется на основе не ментальной и соматической симптоматики и принципа подобия, как в гомеопатии, а анатомо-клинического диагноза исходя из нозологического принципа назначения.
На наш взгляд, представляет интерес оценить с позиции доказательной медицины возможность дополнительного использования препарата Траумель С для лечения келоидных рубцов.
Целью настоящего исследования стала клинико-экспериментальная оценка эффективности препарата Траумель С при лечении келоидных рубцов. Для реализации поставленной цели были сформулированы следующие задачи:
- Провести проспективное рандомизированное открытое сравнительное в параллельных группах клиническое исследование эффективности дополнительного назначения препарата Траумель С для пациентов, которым к общепринятому лечению (2–3 инъекции препарата Кеналог 40 в рубец, 1 раз в месяц в течение первых 3 месяцев) вводили препарат Траумель С под рубец (2 раза в неделю 6 инъекций и одна инъекция через 6 месяцев).
- Установить особенности влияния дополнительного назначения препарата Траумель С на неблагоприятный исход, свидетельствующий о недостаточной эффективности лечения (клинические случаи наличия эритемы, возвышения рубца над уровнем здоровой кожи, неудовлетворенность лечением).
- Оценить на основе общепринятых в доказательной медицине количественных результатов оценки терапевтического эффекта эффективность предлагаемого вмешательства.
- Исследовать in vitro на первичных культурах дермальных фибробластов человека прямое воздействие препаратов Кеналог 40 и Траумель С, как каждого в отдельности, так и при сочетанном их использовании путем введения препарата Траумель С в ростовую среду после предварительного культивирования фибробластов в присутствии Кеналога 40 и последующей смены среды и этапа культивирования без какого-либо воздействия.
Материалы и методы исследования
Обследован 51 пациент: 25 пациентам основной группы по сравнению с 26 контрольной группы дополнительно к общепринятому лечению (2–3 инъекции препарата Кеналог 40 в рубец 1 раз в месяц в течение первых 3 месяцев) вводили препарат Траумель С под рубец 2 раза в неделю 6 инъекций и одна инъекция через 6 месяцев. Количественная оценка вмешательства проводилась через 6 и 12 месяцев.

За неблагоприятный исход, свидетельствовавшщий о недостаточной эффективности лечения, принимали клинические случаи наличия эритемы, возвышения рубца над уровнем здоровой кожи, его плотность, а также неудовлетворенность лечением. Особое внимание обращали на проведение дифференциальной диагностики между рубцами. Критерии включения: пациенты с келоидными рубцами в отсутствие признаков хронической соматической патологии. Критерии исключения: пациенты с нормо-, атро-, гипо- и гипертрофическими рубцами, заболеваниями печени, сердечно-сосудистой и эндокринной систем, кожными болезнями и аллергическими состояниями.
Схема лечения: Кеналог 40 в рубец 1 раз в месяц (в течение первых 3 месяцев), Траумель С под рубец – 2 раза в неделю, 6 инъекций (в течение первых 3 месяцев) и одна инъекция через 6 месяцев наблюдения. Дизайн – проспективное рандомизированное открытое сравнительное контролируемое в параллельных группах клиническое исследование. В течение всего периода исследования из него не выбыл ни один пациент.
При оценке эффекта вмешательств использовали статистические программы Review Manager, а в них – четырехпольные таблицы, которые позволяли вычислять взвешенные (относительно размера включенного в анализ исследования) величины относительных показателей и их доверительные интервалы. Статистическая значимость различий для проверки гипотезы о связи двух качественных признаков в группах обследуемых рассчитывалась непараметрическими методами критерия χ2 с поправкой Йетса или точного критерия Фишера (если в клетках таблицы сопряженности 2×2 числа меньше 5). При представлении результатов оценки вмешательств рассчитывали показатели, рекомендованные редакторами журналов Evidence-Based Medicine, ACP Journal Club, принятые в доказательной медицине [1, 2, 4, 5].

За неблагоприятный исход, свидетельствовавший о недостаточной эффективности лечения, принимали клинические случаи наличия эритемы, возвышения рубца над уровнем здоровой кожи, неудовлетворенность лечением. Составляли таблицу сопряженности, в которой приводили возможные неблагоприятные исходы, свидетельствовавшие о недостаточной эффективности фармакотерапии келоидных рубцов (табл. 1).
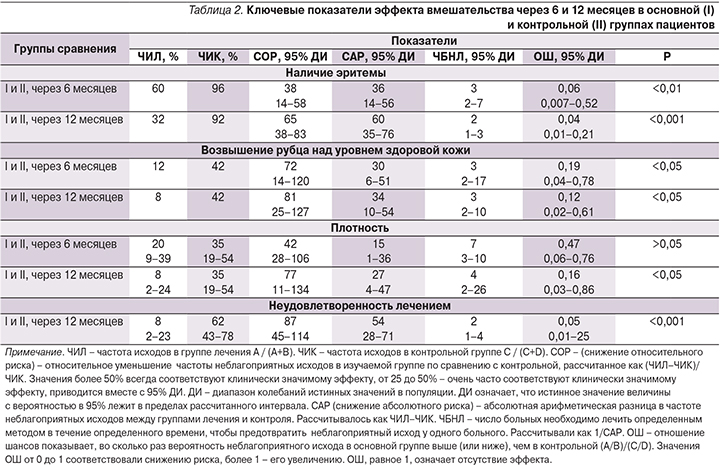
Затем рассчитывали рекомендованные ключевые показатели (табл. 2).
Тестирование in vitro Траумель С и Кеналога 40 на первичных культурах дермальных фибробластов человека
Исследования in vitro на первичных культурах дермальных фибробластов человека выполнены на базе Института экспериментальной медицины и биотехнологии Самарского государственного медицинского университета в лаборатории культивирования клеточных культур.
Для исследования непосредственного действия препаратов Траумель С и Кеналог 40 на фибробласты человека в культуре взяты лекарственные препараты: Траумель С (ампулы по 2,2 мл; производитель Биологише Хайльмиттель Хеель ГмбХ) и Кеналог 40 (ампулы по 1 мл, содержание действующего вещества 40 мг/мл; производитель Бристол-Майерс Сквибб С.р.Л.). Исследования исполнены на первичных культурах дермальных фибробластов человека 4–10-го пассажа. Культуру дермальных фибробластов получали методом первичных эксплантатов из фрагментов кожи абортусов 8–10 недель гестации. Опыты осуществлялись методом прямого контакта. При посеве доза во всех случаях составляла 20 тыс. клеток/см2 (2×104). Контролем служили: 1. Чашки Петри с бессывороточной ростовой средой без исследуемого вещества и фибробластов; 2. Чашки Петри с полной ростовой средой без исследуемого вещества и фибробластов; 3. Чашки Петри с полной ростовой средой и образцами исследуемого вещества, в которые не высевали фибробласты; 4. Чашки Петри с культурой фибробластов, которые пассировали и наблюдали одновременно с экспериментальными, но не подвергали никакому воздействию. Все работы проводили в ламинарном боксе (БАВп-01 «Ламинар-С»).
По предложенному нами дизайну было проведено 3 группы экспериментов: в 1-й и 2-й группах изучали воздействие на культуру фибробластов в течение 5 суток каждого препарата в отдельности; в 3-й группе сначала культивировали фибробласты в течение 5 суток в присутствии препарата Кеналог 40, затем производили смену среды и культивировали клетки без какого-либо воздействия 2 суток, после чего в ростовую среду вводили препарат Траумель С и продолжали культивирование еще 5 суток. Нативную культуру изучали, морфометрировали и фотографировали с помощью инвертированного микроскопа «Биолам П–2-1» при увеличении 100 и 150 (окуляры 10 и 15, объектив 10). Ежедневно проводили визуальные наблюдения и морфометрию нативной культуры. Визуально оценивали целостность монослоя, наличие слущенных клеток в культуральной жидкости, форму и размеры клеток, структуру клеток (состояние цитолеммы, состояние цитоплазмы – наличие вакуолей, зернистости, наличие и состояние отростков, структуру ядра и ядрышек, положение ядра в клетке, количество ядер и ядрышек в клетках). Для определения количества поврежденных клеток в монослое считали 200 клеток в 5 полях зрения, из них отдельно учитывали поврежденные клетки.
Фиксированные 4%-ным раствором параформальдегида препараты окрашивали гематоксилином и эозином, пикрофуксином, орсеином по Унна – Тенцеру. В нефиксированных клетках монослоя выявляли нейтральный жир суданом VI.

Результаты исследования и их обсуждение
Количественные результаты оценки показателей, характеризующих эффект вмешательства изучаемого и обычного методов лечения, представлены в табл. 2.
Как видно из приведенных в табл. 2 результатов исследований, у пациентов основной группы по сравнению с контрольной неблагоприятные исходы, свидетельствовавшие о недостаточной эффективности фармакотерапии келоидных рубцов, наблюдались статистически значимо реже. Высокие значения показателей САР и СОР характеризуют клиническую значимость полученных результатов. Показатели ЧБНЛ и ОШ позволяют утверждать, что при дополнительном назначении препарата Траумель С у каждого 4-го и 5-го пациента может появиться возможность избежать неблагоприятного исхода при лечении келоидных рубцов как через 6, так и через 12 месяцев.
Результаты in vitro исследования прямого воздействия препаратов Кеналог 40 и Траумель С каждого в отдельности и эффекты воздействия Траумель С на фибробласты после предварительного их культивирования в присутствии Кеналога 40 демонстрируются на рис. 1–4 (окраска орсеин) и рис. 5–8 (окраска судан VI). Как видно из приведенных рисунков, обнаруживается очевидная однонаправленная зависимость. Введение Кеналога 40 приводит к нарушению формирования внеклеточного матрикса в культуре фибробластов через 5 суток. Траумель С, введенный в суспензию клеток после Кеналога 40, в значительной степени демонстрирует заметное восстановление морфофункционального состояния фибробластов. Иными словами, установлен не известный ранее факт прямого воздействия препарата Траумель С на клеточном уровне, заключающийся в модуляции морфофункционального состояния фибробластов человека. Результаты клинико-экспериментальной оценки эффективности дополнительного назначения препарата Траумель С открывают перспективу для включения данного комплексного антигомотоксического средства в схемы лечения келоидных рубцов.

Выводы
- В процессе проспективного рандомизированного открытого контролируемого сравнительного в параллельных группах исследования показаны эффективность и целесообразность дополнительного назначения препарата Траумель С для предотвращения неблагоприятных исходов, характеризующих недостаточную эффективность фармакотерапии келоидных руб-цов.
- Исследования in vitro на первичных культурах дермальных фибробластов человека в присутствии препарата Кеналог обнаружили нарушение формирования внеклеточного матрикса в культуре фибробластов через 5 суток.
- Исследования in vitro на первичных культурах дермальных фибробластов человека в присутствии препарата Траумель С показали, что в этих условиях фибробласты практически не страдают, продолжая образовывать сплетения коллагена и способствуя нормальному физиологическому функционированию внеклеточного матрикса.
- Введение в суспензию клеток после кеналога препарата Траумель С в значительной степени приводило к восстановлению морфофункционального состояния фибробластов в культуре клеток.



