Введение
СД – заболевание с постоянной тенденцией роста. По данным Международной диабетической федерации, численность больных СД в мире за последние 10 лет увеличилась более чем в 2 раза. К концу 2021 г. число больных составило 537 млн, а по прогнозам, к 2030 г. возрастет до 643 млн [1]. В 2023 г. на 76-й сессии Всемирной организации здравоохранения (ВОЗ) одобрен Глобальный план действий по профилактике и контролю неинфекционных заболеваний, в котором указаны 6 основных направлений в лечении СД с целью профилактики развития микро- и макрососудистых осложнений: уход за ногами для предотвращения ампутации, скрининг диабетической ретинопатии, гликемический контроль за СД, скрининг альбуминурии, контроль артериального давления и применение статинов. В резолюции ВОЗ также отмечено, что совершенствование лекарственной терапии идет параллельно с инновационными разработками технологий в управлении СД (средства мониторинга и введение инсулина). Также были определены приоритетные задачи в управлении СД к 2030 г.: у 80% пациентов СД должен быть диагностирован, 80% пациентов с диагностированным СД должны иметь хорошо контролируемую гликемию, 80% пациентов с диагностированным СД должны иметь целевые показатели артериального давления, 60% людей с СД в возрасте 40 лет и старше должны получать статины, 100% пациентов с СД 1 типа должны получать инсулинотерапию и проводить самоконтроль уровня глюкозы крови.
В резолюции ВОЗ подчеркнуто, что всем больным СД необходимо исследовать уровень гликированного гемоглобина (HbA1c) для оценки состояния углеводного обмена [2].
Начиная с 1970-х гг. и до настоящего времени HbA1с остается «золотым стандартом», оценивающим эффективность гликемического контроля при СД и маркером риска развития поздних осложнений СД. Его информативность и надежность были неопровержимо подтверждены рядом известных многолетних многоцентровых клинических исследований [3, 4].
НbА1с используется для определения индивидуальных целей лечения пациентам с СД, а с 2011 г. и в качестве диагностического критерия этого заболевания [5].
Однако, несмотря на очевидные достоинства, данный показатель имеет определенные ограничения. В первую очередь НbА1с не отражает колебания гликемии в течение суток и в различные дни, а также периоды гипо- и гипергликемии в конкретные временные интервалы, поскольку дает представление только о среднем уровне глюкозы крови за последние 2–3 месяца как некий «ориентир к действию». Поэтому использование этого показателя как единственного критерия эффективности не позволяет выработать индивидуальную тактику коррекции терапии в каждом клиническом случае и проводить своевременную целевую коррекцию терапии [5].
Более того, информативность НbА1с существенно снижается у пациентов с анемией различного генеза, гемоглобинопатией, при беременности.
В целом на уровень НbА1с нужно опираться при определении тактики ведения пациентов с СД. Кроме того, он остается единственным валидированным индикатором риска развития осложнений. Однако значение этого показателя для выбора схем и доз сахароснижающих препаратов больным СД существенно ограничено [6].
Таким образом, уровень HbA1c не отражает таких важных аспектов, как вариабельность гликемии в течение дня и изо дня в день, а также частоту гипогликемических состояний. Это означает, что достижение цели по уровню НbА1с далеко не в каждой клинической ситуации свидетельствует об эффективности и безопасности проводимой сахароснижающей терапии. Поэтому недостаточно опираться только на уровень HbA1c, т.к., руководствуясь лишь им, ни пациент, ни врач не могут достоверно оценить, в какой период времени значения гликемии были выше верхней границы целевого уровня, а в какой – ниже нижней границы.
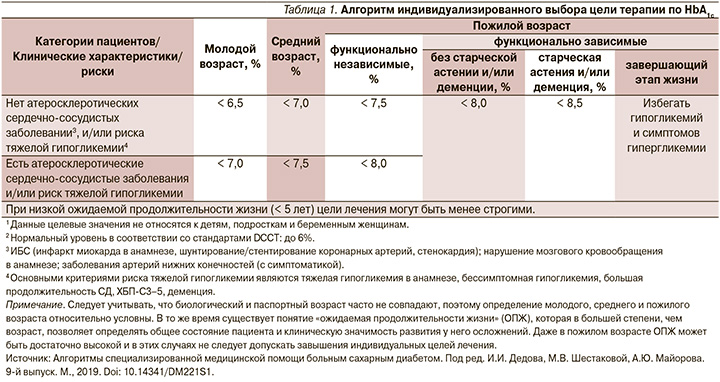
В Российских Алгоритмах специализированной медицинской помощи больным сахарным диабетом (11-й выпуск, 2023) выбор целевого уровня HbA1c зависит от возраста пациента, ожидаемой продолжительности жизни, наличия атеросклеротических сердечно-сосудистых заболеваний и/или риска тяжелой гипогликемии (табл. 1).
Самоконтроль гликемии
Важной опцией эффективной терапии СД является самостоятельный контроль показателей гликемии пациентом в домашних условиях. Самоконтроль способствует достижению и длительному удержание показателей углеводного обмена в целевом диапазоне, является важнейшим фактором, позволяющим снижать риск развития поздних осложнений СД.
Несмотря на использование для лечения СД широкого спектра современных сахароснижающих препаратов, большинство больных не достигают целевых показателей гликемического контроля. В настоящее время средства самоконтроля доступны больным СД, однако приверженность к проведению самоконтроля остается низкой. Только 44% взрослых с СД1 и 24% больных СД2 проводят регулярный самоконтроль в соответствии с рекомендацией врача. Приверженность молодых пациентов к самоконтролю составляет 31–69%. Она выше у обученных пациентов. Без данных самоконтроля невозможно проведение коррекции сахароснижающей терапии. Это является одной из основных причин того, что пациенты не достигают целей терапии [7, 8].
Для больных СД рекомендуются индивидуальные цели лечения не только по уровню НbА1с, но и по показателям гликемии натощак (ГПН), постпрандиальной гликемии (ППГ). Целевые уровни глюкозы плазмы натощак/перед едой/на ночь/ночью соответствуют по значению целевым уровням HbA1c. Так, значения глюкозы плазмы через 2 часа после начала приема пищи менее 8,0 ммоль/л соответствуют HbA1c менее 6,5%, а далее увеличивается на 1 ммоль/л на каждые 0,5% HbA1c (табл. 2) [5]. В 2013 г. Международная диабетическая федерация предложила увеличение целевого уровня HbA1c до 8,5% у пациентов пожилого возраста, имеющих деменцию или физически ослабленных, которые не могут самостоятельно себя обслуживать.
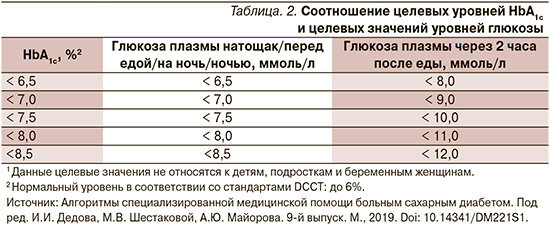
Каждого пациента необходимо проинформировать о его индивидуальном целевом уровне НbА1с, ГПН/перед едой/на ночь/ночью и глюкозы плазмы через 2 часа после начала приема пищи, чтобы он знал, к чему надо стремиться [5].
В течение многих лет подходы к терапии СД основывались на понимании взаимосвязи между HbA1c с отдаленными исходами данного заболевания вне зависимости от его типа. В классических исследованиях среди популяций пациентов СД1 (DCCT) и СД2 (UKPDS) было продемонстрировано, что снижение уровня HbA1c ассоциировано с клинически значимым снижением риска развития микрососудистых осложнений и ряда сердечно-сосудистых заболеваний [3, 4].
Недостижение целевого уровеня НbА1с свидетельствует о необходимости изменения дозы препаратов или схемы терапии. Коррекцию дозы инсулина и сахароснижающих препаратов врач проводит на основании показателей гликемии, которые пациент предоставляет ему на визите. В свою очередь, зная результаты самоконтроля, врач предоставляет пациенту рекомендации по питанию, физической активности, коррекции терапии.
В лечении СД огромную роль играет эффективное взаимодействие между врачом и пациентом, способствующее достижению индивидуальных целевых показателей гликемии. Важное значение в достижении целей терапии имеют знания и навыки, благодаря которым пациент может управлять своим заболеванием, а также достаточный уровень мотивации к их использованию. В работу врача входит не только проведение обследования и подбор терапии, но и осуществление процесса обучения и мотивации пациента на достижение целей терапии. Особое место в концепции лечения СД отводится повышению качества жизни пациентов, адаптации человека с диабетом в обществе. Крайне важно изменить поведение больного и научить его грамотно управлять своим состоянием за счет активного вовлечения в лечебный процесс, невозможный без мониторинга гликемии.
В 1999 г. началось внедрение в клиническую практику непрерывного мониторинга гликемии (НМГ) – новой опции контроля за гликемией.
В феврале 2017 г. на Конгрессе ATTD (Advanced Technologies and Treatment for Diabetes) группой экспертов принят Международный консенсус по использованию НМГ. Ниже приведены наиболее важные положения консенсуса, которые распространились и на данные, получаемые при самоконтроле гликемии с помощью глюкометра с мобильным приложением.
1) Поскольку высокая вариабельность гликемии служит предиктором развития гипогликемии и сопровождается повышенным риском летального исхода, рекомендуется оценивать стандартное отклонение, коэффициент вариации (КВ) и среднюю амплитуду колебаний глюкозы в качестве показателей вариабельности гликемии. КВ является предпочтительным способом и рассчитывается как отношение стандартного отклонения к среднему значению величины, измеряемое в процентах. Гликемия считается стабильной при КВ менее 36% и нестабильной при КВ более 36%.
2) Рекомендовано использовать параметр «time in range» – время нахождения в диапазоне целевых значений гликемии (ВЦД) (3,9– 10,0, реже – 3,9–7,8 ммоль/л), дающий более развернутую информацию о текущем состоянии гликемического контроля по сравнению с HbA1c.
3) Следует рассчитывать в процентах периоды пребывания в следующих диапазонах: 2-й уровень гипогликемии (ВНЦ2) (менее 3,0 ммоль/л), 1-й уровень гипогликемии (ВНЦ1; 3,9–3,0 ммоль/л), ВЦД (3,9–10,0 или 3,9–7,8 ммоль/л), 1-й уровень гипергликемии (ВВЦ1; 10,0–13,9 ммоль/л), 2-й уровень гипергликемии (ВВЦ 2; более 13,9 ммоль/л). Этот метод весьма удобен для оценки эффективности лечения, а также помогает пациентам увидеть, как изменяются частота и выраженность гипо- и гипергликемии на фоне лечения.
4) Стоит также выделять периоды времени: период сна (00.00–06.00), пробуждения (06.00–12.00), весь день (00.00–24.00), что позволяет более прицельно проводить коррекцию терапии [9] (табл. 3).
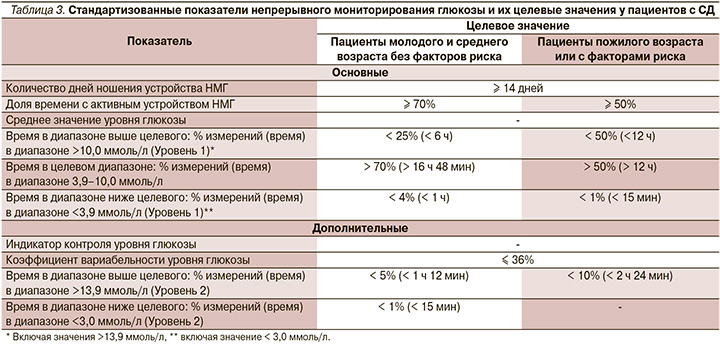
Для пациентов, осуществляющих самоконтроль с помощью НМГ, в т.ч. флеш-мониторирования глюкозы (ФМГ), в качестве целей гликемического контроля дополнительно используются стандартизированные показатели, включая время в диапазонах глюкозы: время в целевом диапазоне (ВЦД), время выше целевого диапазона (ВВЦ), время ниже целевого диапазона (ВНЦ) [5].
В настоящее время данные времени в диапазонах можно получать при самоконтроле гликемии с помощью глюкометра с мобильным приложением.
В литературе представлены данные клинических исследований, показывающие взаимосвязь между ВЦД и риском развития микро- и макрососудистых осложнений (табл. 4) [10–15].

В 2021 г. Lu J. et al. провели изучение влияния ВЦД на риск смерти при СД2. Всего в исследование были включены 6225 человек с СД2. Исходно ВЦД измерялся с помощью НМГ. По уровню ВЦД пациенты были разделены на четыре группы: >85%, 71–85%, 51–70% и ≤50%. Модели регрессии пропорциональных рисков Кокса использовались для оценки связи между различными уровнями ВЦД и рисками смертности от всех причин и сердечно-сосудистых заболеваний (ССЗ).
Исходный средний возраст участников составлял 61,7 года. За период наблюдения (в течение 6,9 года) выявлено 838 случаев смерти, 287 из которых были связаны с ССЗ. Скорректированные по многим переменным коэффициенты риска, вызванные различными уровнями ВЦД (>85% [референтная группа], 71–85%, 51–70% и ≤50%), составили 1,00, 1,23 (95% ДИ: 0,98–1,55), 1,30 (95% ДИ: 1,04–1,63) и 1,83 (95% ДИ: 1,48–2,28) для смертности от всех причин (р<0,001) и 1,00, 1,35 (95% ДИ: 0,90–2,04), 1,47 (95% ДИ: 0,99, -2,19) и 1,85 (95% ДИ: 1,25–2,72) для смертности от ССЗ (р=0,015) соответственно. Таким образом была показана связь более низкого ВЦД с повышенным риском смертности от всех причин и ССЗ среди пациентов с СД2, что подтверждает ценность ВЦД в качестве суррогатного маркера долгосрочных неблагоприятных клинических исходов (рис. 1) [16].
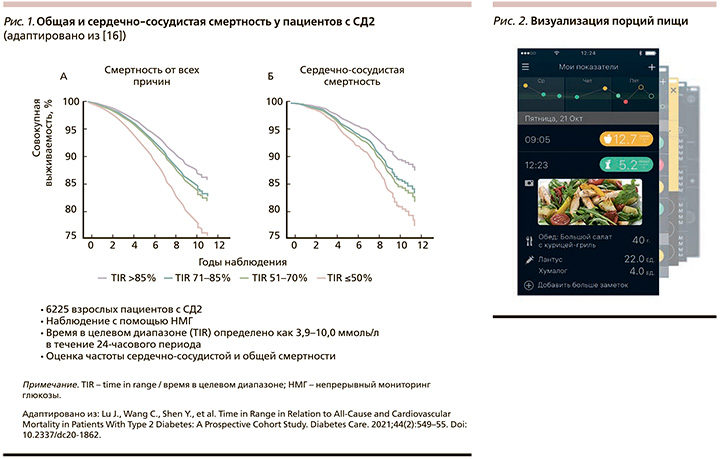
Таким образом, ВЦД может служить эталонным показателем для краткосрочного контроля уровня глюкозы крови, отражая эффективность регуляции уровня глюкозы в крови и прогнозируя риск диабетических микрососудистых осложнений.
В настоящее время подобные отчеты формируются в мобильных приложениях глюкометров.
Сохраняется актуальность более широкого использования современных средств мониторинга гликемии с мобильными приложениями при проведении самоконтроля и обучения пациентов работе с ними.
Появление глюкометров, передающих данные на мобильное приложение для смартфона или айфона, предоставило реальную возможность улучшения гликемического контроля у больных СД, позволив пациентам и врачам обмениваться информацией дистанционно (при помощи текстовых сообщений или электронной почты). Это может приводить к минимизации частоты обращений в амбулаторные медицинские учреждения [17]. Показано, что мобильные медицинские технологии (mHealth) способны улучшать показатели HbA1c, а также эффективны для установления дистанционного обмена информацией между пациентами и врачами [18].
По представленным данным опроса в Интернете наиболее часто применяемой технологией является обмен текстовыми сообщениями (СМС). Использование данной опции в мобильных медицинских технологиях (mHealth) также может способствовать большему вовлечению определенных категорий пациентов в управление диабетом [19].
В настоящее время мобильные технологии получили широкое распространение. Имеются данные о возможности их использования для достижения индивидуальных целей гликемического контроля у пациентов как с СД1, так и с СД2. По результатам мета-анализа, технологии, основанные на использовании мобильных телефонов, позволили снизить HbA1c на 0,5% за 6 месяцев с более выраженным снижением HbA1c у больных СД2 (0,8%) по сравнению с пациентами с СД1 (0,3%) [20]. Кроме того, в обзоре результатов 13 исследований установлена статистически значимая позитивная динамика показателей гликемического контроля у пациентов с СД2, использующих для обмена данными короткие сообщения, по сравнению c очными визитами к врачу [21].
Новые достижения в области облачного программного обеспечения и мобильных приложений по контролю СД, которые используются совместно с глюкометрами, позволили разработать новые модели взаимодействия между пациентами и врачами [22]. Современные глюкометры-системы дают возможность людям с СД самостоятельно оценивать важнейшие параметры обмена веществ с точностью, близкой к лабораторной в привычной для пациента обстановке. Именно самоконтроль гликемии является наиболее важной опцией для подбора терапии, чем исследования гликемии, выполняемые в условиях поликлиники или стационара.
В настоящее время разрабатывается приложение Сателлит Online для глюкометра Сателлит. Пользователям глюкометра OneTouch Verio доступно мобильное приложение OneTouch Reveal®. Соединяется с глюкометрами (OneTouch Verio Reflect®, OneTouch Select Plus Flex®) с помощью Bluetooth.
В реальной клинической практике была оценена эффективность использования глюкометра OneTouch Verio Reflect с приложением OneTouch Reveal у 55 тыс. больных СД с инвалидностью. Показано, что у пациентов с СД1 и СД2 ВЦД улучшалось на 7,8% (с 57,9 до 65,7%) и 12,0% (с 72,8 до 84,8%) соответственно через 180 дней, а ВВЦ снизилась на -8,4% (с 37,9 до29,5%) и -12,2% (с 26,2 до14,1%) без клинически значимых изменений в процентном соотношении ВНД (р<0,0005) [23].
Одним из таких современных глюкометров-систем является Contour Plus One (Контур Плюс Уан) с мобильным приложением – Contour Diabetes (Контур Диабитис).
Глюкометр-система оснащена набором функций и возможностей, особенно важных для пациентов на интенсифицированной инсулинотерапии, таких как:
- дата и время;
- установка целевого диапазона гликемии для интерпритации результатов;
- использование отметки «до еды» и «после еды». Контроль гликемии натощак помогает оптимизировать дозу базального инсулина, показатели гликемии «до еды» и «после еды» – дозу болюсного инсулина. Отметки о еде подскажут, как различные виды пищи и размеры порций влияют на уровень глюкозы крови;
- добавление фотографии употребляемой пищи, что позволяет точнее учитывать содержание углеводов (рис. 2);
- средние значения гликемии вместе с показателями гликемии натощак, поможет оптимизировать дозу базального инсулина;
- тренды гликемии. Эта функция позволяет быстрее и точнее анализировать показатели и выявлять тенденции изменений гликемии по сравнению с обычным дневником самоконтроля. При выявлении повторяющихся эпизодов гипо- (не менее 2 эпизодов за трехчасовой интервал) или гипергликемии (не менее 3 эпизодов за трехчасовой интервал) на протяжении 5 дней, глюкометр-система автоматически выводит информацию с предупреждением на экран. Это позволяет сокращать время анализа показателей гликемии, количество неправильных интерпретаций результатов, а также снижать риск развития тяжелых гипогликемических состояний;
- технология «Второй Шанс». Она позволяет добавлять на тест-полоску кровь из той же капли, не делая еще один прокол, если первого образца оказалось недостаточно. Это никак не отражается на точности измерений. После нанесения тестируемого образца на тест-полоску – для чего надо лишь коснуться ее заборным концом капли крови, которая втянется сама за счет силы капиллярного всасывания, – прибор оценит, достаточен ли объем для корректного тестирования. Если нет – прибор дважды издаст звуковой сигнал, а на экране появится изображение недозаполненной тест-полоски: теперь на дополнительное нанесение крови у пациента имеется 60 секунд.
- функция «Умная подсветка» позволяет быстро оценить полученный результат.
В приложении Контур Диабитис к результатам измерений глюкозы крови можно добавлять информацию о лекарственной терапии, физической активности, введении инсулина, устанавливать напоминания, строить графики для удобного просмотра всех показателей. В данном приложении можно сформировать сводный отчет, который может быть отправлен врачу по электронной почте либо врач может ознакомиться с ним онлайн (при предоставлении доступа).
«Облачное» приложение позволяет врачам наблюдать за течением заболевания у пациентов, обеспечивает возможность дистанционного консультирования, суммирует результаты измерения гликемии и формирует аналитические отчеты (рис. 3).
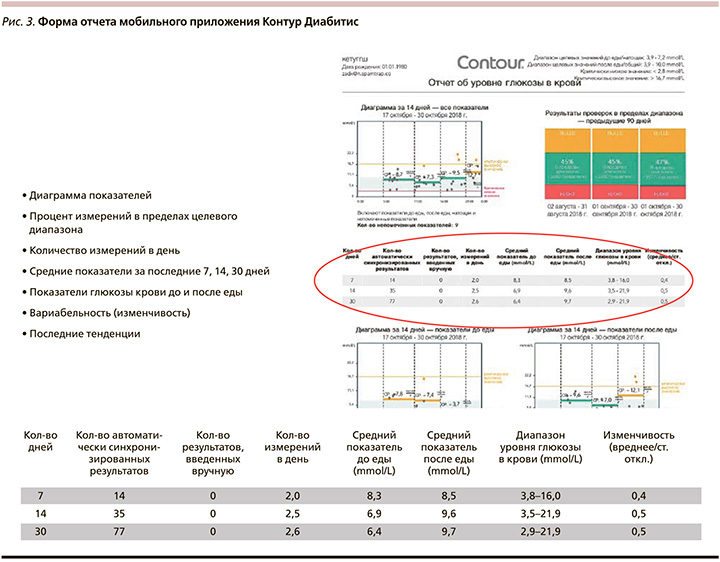
Использование опций, заложенных в мобильном приложении, позволяет улучшать показатели гликемии.
Проведена оценка результатов использования приложения Contour Diabetes у 5870 пациентов с СД.
Отношение рисков иметь хотя бы один эпизод гипергликемии в течение первых 30 дней и через 180 дней составило 1,56 (95% ДИ: 1,32–1,91). Отношение рисков иметь хотя бы один эпизод гипогликемии в течение первых 30 дней и через 180 дней составило 2,47 (95% ДИ: 2,02–3,07). Частота тестирования через 180 дней увеличилась до 4,48 раза в день по сравнению с 2,03 раза в сутки в первые 30 дней (p<0,0001). Вероятность развития гипогликемии снизилась на 60%, гипогликемии на 36% [24].
В настоящее время многие пациенты не фиксируют результаты самоконтроля на бумажных носителях. Интенсивное дистанционное взаимодействие между врачом и пациентом позволяет осуществлять мониторинг показателей гликемии и оперативно проводить коррекцию лечения, оценивать его эффективность. Сам факт того, что пациент знает о доступности показателей гликемии его врачу, служит мощным стимулом для соблюдения рекомендаций, изменения образа жизни, повышения мотивации на достижения цели лечения.
В этом плане мобильное приложение Контур Диабитис является электронным дневником самоконтроля, который автоматически собирает и сохраняет результаты, показывает данные в удобном формате (диаграммы, графики, тренды, цветовые подсказки), позволяет формировать и делиться отчетами (e-mail, смс и др.), быстро выявлять потенциальные проблемы, способствует вовлечению пациента в управление диабетом, экономит время на приеме врача (рис. 4).
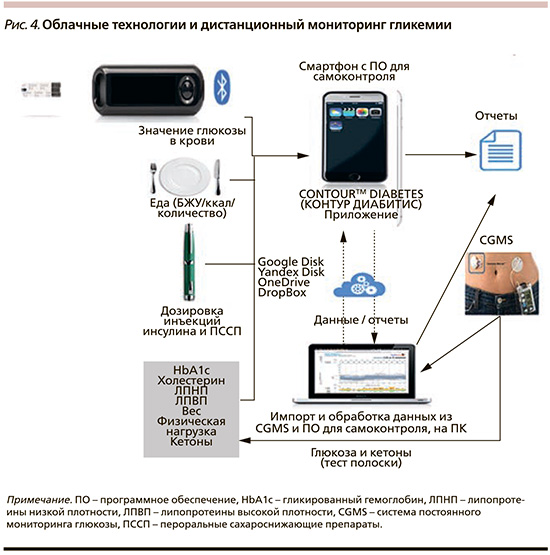
Заключение
Таким образом, современные глюкометры-системы с мобильным приложением позволяют более оперативно управлять гликемией, повышать приверженность пациентов к активному управлению заболеванием, достигать цели лечения с использованием инновационных технологий.
Вклад авторов. М.Б. Анциферов – разработка дизайна статьи, утверждение рукописи для публикации. О.М. Котешкова – обзор публикаций по теме статьи, написание текста рукописи. Д.М. Анциферова – перевод на английский язык, анализ собранных данных. Н.А. Демидов – сбор данных литературы.



