Введение
Наиболее обсуждаемыми вопросами применения антигистаминных препаратов (АГП) являются вопросы безопасности их высоких доз (например, при крапивнице) и пролонгированной терапии пациентов с аллергическими заболеваниями. Длительные курсы АГП возможны в отсутствие рисков побочных эффектов и развития тахифилаксии. Благодаря структурной схожести с гистамином антагонисты Н1-гистаминовых рецепторов связываются с рецепторами гистамина на клетках разных тканей, конкурентно блокируя Н1-рецепторы. Согласно классификации, принятой Европейской академией аллергологии и клинической иммунологии (EAACI, 2003), выделяют два поколения антигистаминных средств: первое поколение, или седативные АГП, и второе – неседативные АГП [1]. К препаратам 1-го поколения относятся супрастин, тавегил, димедрол, перитол, диазолин, фенкарол, фенистил и др. Большинство из них были синтезированы в середине прошлого века, но с успехом применяются до настоящего времени. К особенностям этой группы препаратов можно отнести короткую продолжительность терапевтического действия (1,5–6 часов), высокую липофильность, обеспечивающую проникновение через гематоэнцефалический барьер и нарушение когнитивных функций, усиливающееся при совместном применении с алкоголем или седативными средствами [2]. Неполное связывание с Н1-рецепторами (30%) обусловливает высокие терапевтические дозы и частую кратность приема этих препаратов, а также быстрое развитие тахифилаксии к ним. Качество сна при терапии седативными антигистаминными препаратами ухудшается. Седативные АГП (за исключением доксиламина) угнетают REM (rapid eye movement)-фазу сна, после чего вызывают выраженный синдром отмены. В результате сон становится прерывистым (фрагментация сна), нарушается сердечный ритм, развивается тканевая гипоксия и нарушение дыхания во сне (апноэ). Это приводит к дневной сонливости, снижению дневной активности и нарушению когнитивной функции. При апноэ во сне повышается риск внезапной смерти [3].
Еще одним недостатком АГП 1-го поколения является низкая избирательность действия: помимо Н1-гистаминовых рецепторов они блокируют и рецепторы других типов: М-холинорецепторы, α-адренорецепторы, серотониновые, брадикининовые рецепторы. Именно поэтому АГП 1-го поколения имеют ряд серьезных ограничений к применению пациентами с глаукомой, бронхиальной астмой, доброкачественной гиперплазией предстательной железы, сердечно-сосудистой патологией и т.д. Таким образом, АГП 1-го поколения не могут применяться длительными курсами.
АГП 2-го поколения представляют собой разнородную группу, прежде всего в силу особенностей их метаболизма. Среди АГП 2-го поколения выделяют две подгруппы:
- «метаболизируемые», оказывающие терапевтический эффект только после прохождения метаболизма в печени изоферментом CYP 3A4 системы цитохрома Р-450 с образованием активных соединений.
К ним относятся лоратадин, эбастин, терфенадин, астемизол.
- «активные метаболиты» – препараты, поступающие в организм сразу в виде активного вещества (цетиризин, левоцетиризин, дезлоратадин, фексофенадин).
Индивидуальной вариабельностью активности системы цитохрома Р-450 может быть объяснена различная эффективность «метаболизируемых» АГП у разных лиц. При недостаточном метаболизме также возрастает риск побочных токсических эффектов со стороны сердечно-сосудистой системы (удлинение интервала QT и нарушение желудочкового ритма), что было отмечено у терфенадина и астемизола. «Активные метаболиты» обладают более высоким профилем безопасности, при этом их эффект более предсказуем и не зависит от активности ферментов системы цитохрома Р-450, поэтому их применение предпочтительно.
Крайне важным в лечении иммунозависимых и аллергических дерматозов являются высокое сродство АГП 2-го поколения к Н1-рецепторам, быстрое начало действия, длительность эффекта до 24 часов, высокая избирательность действия. Эти препараты не проникают через гематоэнцефалический барьер, поэтому практически не вызывают сонливости. Кроме того, особенно важен дополнительный противоаллергический эффект за счет стабилизации мембраны тучных клеток, уменьшения экспрессии молекул адгезии (ICAM-1), подавления индуцированного эозинофилами выделения интерлейкина-8, ГМ-КСФ и sICAM-1 из эпителиальных клеток, поэтому они более эффективны, чем препараты 1-го поколения [4].
Результаты клинических исследований и реальная практика свидетельствуют: «золотым» стандартом среди АГП заслуженно считается цетиризин – первый высокоизбирательный блокатор Н1-рецепторов. Считается, что для пациентов, плохо отвечающих на терапевтическое действие других АГП, предпочтителен именно цетиризин [5]. Сродство цетиризина к Н1-рецепторам выше, чем у лоратадина, и такое же как астемизола, терфенадина и гидроксизина. При этом специфичность связывания Н1-рецепторов оказывается весьма высокой: даже в высоких концентрациях цетиризин не блокирует серотониновые (5-НТ2), дофаминовые (D2), М-холинорецепторы и α1-адренорецепторы [5]. Действие цетиризина распространяется не только на раннюю, но и на позднюю фазу аллергической реакции. Цетиризин тормозит in vitro активацию эозинофилов, вызванную интерлейкином-8, лейкотриеном В4 и С5а-компонентом комплемента, хемотаксис этих клеток, вызванный фактором активации тромбоцитов или хемотаксическим агентом, – формилметионил-лейцил-фенилаланином. В аналогичных концентрациях цетиризин тормозит стимулированную специфическим аллергеном цитотоксичность тромбоцитов. В терапевтических дозах цетиризин тормозит выход гистамина в «кожную камеру», вызванный длительным контактом специфического аллергена с кожей чувствительного к нему пациента. В последнее время получены сведения, иллюстрирующие выраженное тормозящее действие цетиризина на персистирующее воспаление в ткани и перестройку профиля продуцируемых цитокинов.
Кроме того, в отличие от других препаратов, применяемых при кожных проявлениях аллергии, цетиризин не только блокирует H1-гистаминовые рецепторы, но и подавляет кожный ответ на тромбоцит-активирующий фактор. Это подтверждено результатами многочисленных клинических сравнительных исследований: способность кумулироваться в кожных покровах позволяет препарату купировать зуд и гиперемию более эффективно, чем эбастин, эпинастин, терфенадин, фексофенадин и лоратадин [6].
Левоцетиризин – не только мощное антигистаминное средство последнего поколения, но оно обладает и противоаллергическими/противовоспалительными свойствами, часть из которых не связана с блокадой H1-рецепторов. Он эффективно подавляет кожную аллергическую реакцию, и его ингибиторная активность коррелирует с высокой занятостью рецепторов [3]. Ряд исследований показывает, что относительно высокие концентрации левоцетиризина на клеточной поверхности в рецепторных участках обусловливают выраженность эффекта и длительную активность препарата. Левоцетиризин создает высокие концентрации в коже. Он практически не проникает через гематоэнцефалический барьер, его седативный потенциал еще меньше, чем у цетиризина, лоратадина и дезлоратадина [7]. Клинически значимые взаимодействия с пищей и лекарственными препаратами отсутствуют [8]. Левоцетиризин достигает максимальных концентраций в плазме крови за 0,9 часа, быстрее других АГП, что способствует более быстрому началу купирования симптомов аллергии [6].
По результатам сравнительных исследований, левоцетиризин в дозе 5 мг значимо эффективнее и быстрее, чем дезлоратадин в дозе 5 мг, действует на симптомы хронической идиопатической крапивницы. Левоцетиризин сильнее, чем дезлоратадин, подавляет воспаление, т.к. он значительнее снижает уровень таких провоспалительных цитокинов, как интерлейкин-1β и интерлейкин-8. Установленное клиническое преимущество левоцетиризина над дезлоратадином при применении в дозе 5 мг 1 раз в сутки утром может служить обоснованием применения левоцетиризина в дозе 5 мг в качестве предпочтительного варианта лечения взрослых пациентов с хронической идиопатической крапивницей [3].
Самым назначаемым препаратом цетиризина является Цетрин (по данным независимой аналитической базы IPSOS Comcon 2 кв., 2021). Препарат начинает действовать быстро (уже через 20 минут) и продолжительно, обладает хорошим профилем безо-пасности [6]. Цетрин практически не метаболизируется в организме. Максимальная концентрация в сыворотке достигается через час после приема, при продолжительном применении не накапливается в организме. Цетрин полностью биоэквивалентен оригинальному препарату [9].
Антигистаминный препарат Аллервэй также имеет доказанную биоэквивалентность референтному препарату левоцетиризина [10], а также собственные исследования по эффективности [17]. По сравнению с рядом АГП 2-го поколения у препарата Аллервэй зарегистрирован больший перечень показаний: аллергический ринит, крапивница, аллергический конъюнктивит, поллинозы, аллергодерматозы, сопровождающиеся зудом и высыпаниями. В сравнительном исследовании клинической эффективности и фармакоэкономических параметров препаратов левоцетиризина для пациентов с хронической крапивницей показана наилучшая эффективность у оригинального препарата и у Аллервэя, при этом по фармакоэкономическим характеристикам Аллервэй – несомненный лидер [8].
Таким образом, данные об эффективности и безопасности АГП 2-го поколения из группы «активных метаболитов» делают их наиболее приемлемыми для длительного использования в клинической практике, а цетиризин и левоцетиризин соответствуют требованиям к применению АГП для длительного контроля аллергических заболеваний или крапивницы, в ситуациях, когда это необходимо.
Уже имеются данные об эффективности и безопасности длительного применения цетиризина и левоцетиризина в отношении пациентов с различными аллергическими заболеваниями. Так, в двойном слепом плацебо-контролируемом многоцентровом исследовании, включившем 551 пациента с хроническим ринитом и сенсибилизацией к пыльце трав и клещам домашней пыли, Claus Bachert et al. изучали эффективность и безопасность левоцетиризина в дозе 5 мг/сут в течение 6 месяцев. Выводы авторов: применение левоцетиризина способствует улучшению качества жизни и ослаблению симптомов заболевания, а также позволяет снижать общие затраты на лечение. Также была отмечена высокая безопасность левоцетиризина в дозе 5 мг/сут. в течение 6 месяцев лечения, что подтверждалось более низким по сравнению с плацебо количеством вышедших из исследования по причине развития побочных эффектов пациентов (160,27 против 108,18) [11].
В другом исследовании проанализировано влияние длительного использования цетиризина на тяжесть, естественное течение и лечение атопического дерматита у детей. В проспективном двойном слепом рандомизированном плацебо-контролируемом исследовании с участием 817 детей (в возрасте от 12 до 24 месяцев) показана безопасность применения цетиризина в дозе 0,25 мг/кг в течение 18 месяцев. Авторы сделали вывод, согласно которому с учетом доказанной безопасности цетиризина длительное использование этого препарата может помочь сократить продолжительность применения и количество топических кортикостероидов, используемых при лечении детей с атопическим дерматитом [12].
Данные рандомизированного двойного слепого параллельного группового и плацебо-контролируемого исследования цетиризина на 343 детях младшего возраста (от 12 до 24 месяцев) с массой тела 8–20 кг также подтверждают безопасность его применения на протяжении 18 месяцев. Пациенты получали пероральные капли цетиризина в дозе 0,25 мг/кг 2 раза в день в течение 18 месяцев. Концентрацию активного энантиомера левоцетиризина в плазме определяли в образцах крови, собранных на 3-й, 12 и 18-й месяцы. Фармакокинетика и безопасность препарата соответствовали таковой у взрослых, принимающих рекомендуемую дозу 5 мг один раз в сутки [13].
В рандомизированном двойном слепом плацебо-контролируемом исследовании с участием 510 детей с атопией в возрасте от 12 до 24 месяцев 255 пациентов, получавших левоцетиризин в дозе 0,125 мг/кг 2 раза в день в течение 18 месяцев, показана высокая безопасность препарата. Число детей с серьезными побочными эффектами было на терапии левоцетиризином 12,2% против 14,5% в группе плацебо; с побочными эффектами, связанными с приемом лекарств: левоцетиризин – 5,1% против плацебо 6,3%; а также с побочными эффектами, которые привели к прекращению приема исследуемого препарата (левоцетиризин – 2,0% против плацебо 1,2%). Наиболее частые неблагоприятные события, связанные с инфекциями верхних дыхательных путей, преходящими симптомами гастроэнтерита или обострениями аллергических заболеваний. В ходе исследования седативный эффект препарата не отмечен, а также отсутствовало развитие тахифилаксии. Таким образом, подтверждена долгосрочная безопасность левоцетиризина для детей раннего возраста с атопией [14].
В современных протоколах терапии крапивницы при недостаточной эффективности АГП в стандартных дозах разрешено увеличивать суточную дозировку до 4-кратной. В двойном слепом рандомизированном исследовании с включением 80 взрослых пациентов с хронической крапивницей увеличение дозы левоцетиризина с 5 до 20 мг в сутки повысило эффективность терапии, но не повлекло появления седативного эффекта препарата [18].
Методы
Основной профиль пациентов, требующих длительные курсы применения АГП в дерматологии, – это хроническая крапивница и хронические аллергические заболевания. Большинству пациентов с хронической крапивницей рекомендуется 3–6 месяцев регулярной терапии (степень доказательности D) [15, 16] с возможной периодической отменой препарата в отсутствие симптомов заболевания. Для пациентов с длительным анамнезом крапивницы лечение возможно в течение 6–12 месяцев с постепенной отменой препаратов. Пациентам с интермиттирующими, эпизодически появляющимися симптомами возможно назначение терапии «по требованию» или профилактически.
Под нашим наблюдением находились 27 пациентов с хронической крапивницей (табл. 1).
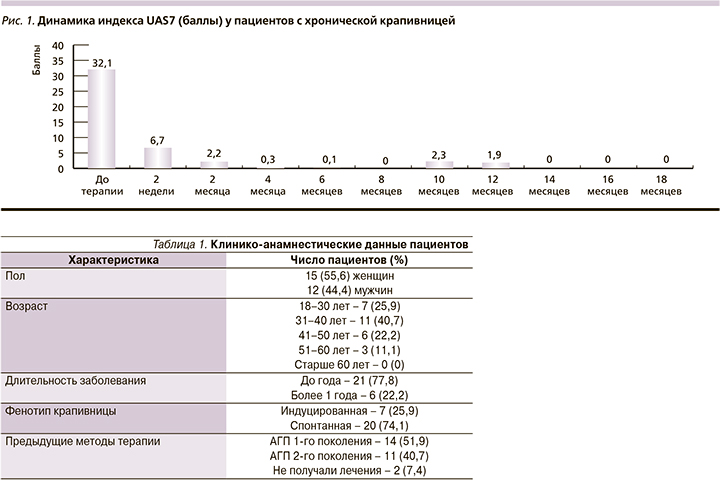
Все пациенты получали левоцетиризин в дозе 5 мг в сутки, длительность приема препарата зависела от купирования клинической симптоматики. Для оценки эффективности терапии использовалась высоковалидная шкала UAS7, или Индекс активности крапивницы. UAS7 предполагает суммарную оценку основных симптомов заболевания (количество высыпаний и интенсивность зуда) самим пациентом каждые 24 часа за 7 последовательных дней. В работе UAS7 подсчитывался 1 раз в месяц за 7 последовательных дней. Сумма баллов за сутки – от 0 до 6, за неделю – максимум 42 балла. Помимо оценки активности заболевания исследовалось качество жизни с учетом индекса качества жизни (ДИКЖ): максимальное значение – 30 баллов (сильное отрицательное влияние на качество жизни).
Для обработки цифрового материала применялись стандартные медицинские статистические методы: высчитывание среднеарифметического значения (Х), квадратичного отклонения (σ), критерий Стьюдента (t).
Результаты исследования
Результаты применения левоцетиризина пациентами с хронической крапивницей представлены в табл. 2 (рис. 1, 2).
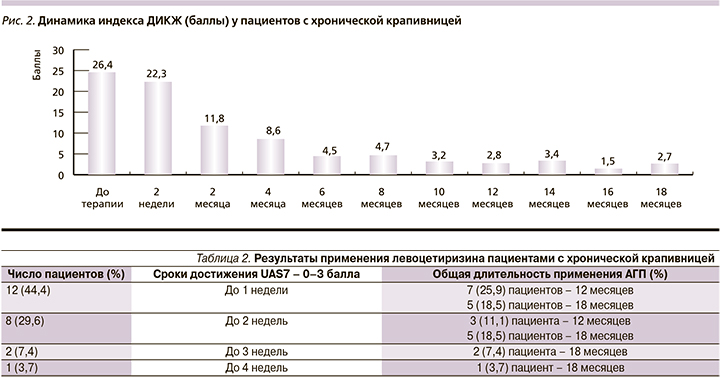
Если пациенты не достигали контроля над заболеванием (UAS7 больше 3 баллов) на протяжении 4 недель, проводилась смена тактики ведения (повышение дозы препарата или добавление омализумаба). В нашем наблюдении таких пациентов было 4 (14,8%).
Выводы
- АГП 2-го поколения являются препаратами выбора при лечении больных хронической крапивницей (индуцированной, спонтанной), при этом в большинстве случаев пациенты нуждаются в длительной терапии АГП.
- Для длительных курсов АГП следует отдавать предпочтение наиболее безопасным препаратам. К их числу относятся цетиризин и левоцетиризин, показавшие свою безопасность в многочисленным плацебо-контролируемых исследованиях, в т.ч. и у детей раннего детского возраста.
- Результаты наблюдательного исследования показали высокую эффективность и безопасность применения левоцетиризина для пациентов с различными формами хронической крапивницы в стандартной дозировке (5 мг в сутки) на протяжении 12–18 месяцев.



