При различных болезнях органов дыхания (острые и хронические бронхиты, бронхиальная астма, бронхоэктатическая болезнь и многие другие), как правило, назначаются специальные препараты, которые влияют на кашель и разжижают мокроту. Кашель как защитный рефлекс обеспечивает очищение слизистой респираторного тракта от вирусов, бактерий, инородных частиц, аллергенов и др. не только при полном здоровье, но и в момент болезни. Поэтому при заболеваниях, протекающих с наличием мокроты, назначать препараты, купирующие кашель, противопоказано. Купировать защитный кашлевой рефлекс разрешается только в конкретных случаях и по особым показаниям, например при коклюше, коревом трахеите, при оперативном вмешательстве, в реанимации или при состоянии ребенка, которое крайне осложняет его самочувствие.
Еще один защитный механизм, придуманный природой, – это слизь, или т.н. мокрота, которая обязательно в небольшом количестве должна изнутри выстилать бронхиальное дерево. В мокроте оседают вредоносные агенты, которые потом эвакуируются с помощью кашля. По характеру слизи можно предварительно судить об этиологии воспаления: например, при аллергии слизь обычно прозрачная, тягучая, «стекловидная». При вирусной инфекции она жидкая и прозрачная или белого цвета. Можно думать о бактериальном воспалении, если слизь вязкая, густая, желто-зеленого цвета. Бокаловидные клетки слизистой оболочки бронхов в момент воспаления (аллергического, инфекционного или иммунного) начинают усиленно продуцировать дополнительную слизь (или мокроту). В дыхательных путях количество мокроты не только увеличивается, но и изменяются ее реологические свойства в сторону сгущения. Мокрота становится вязкой, теряет эластичность, нарушаются ее адгезивные свойства. Логично, что в такой момент терапевтическая тактика сводится к улучшению качества мокроты, нормализации ее химических свойств, что приводит к восстановлению дренажной функции бронхов и постепенному выздоровлению. Качество мокроты также отрицательно влияет на работу мукоцилиарного транспорта. Вязкая мокрота блокирует работу мерцательного эпителия, что приводит к еще большему застою слизи, т.н. мукостазу, появляется влажный кашель, при котором можно выслушать влажные хрипы в легких.
С целью устранения этой ситуации обычно врач из трех групп лекарственных средств выбирает препараты, которые стимулируют откашливание, – откашливающие средства; муколитические препараты; комбинированные препараты (содержат 2 или более компонентов из разных групп). При этом необходимо учитывать особенности и нежелательные явления каждого лекарственного средства, действуя по принципу «максимум лечебного эффекта и минимум побочных эффектов». Важно отметить, что само по себе повышенное образование слизи и выведение ее из бронхиального дерева не является самостоятельным «заболеванием», а представляет лишь симптом или признак разнообразных патологий респираторной системы. Поэтому муколитические препараты должны применяться в качестве симптоматического лечения.
Общая проблема откашливающих средств заключается в следующем: они значительно увеличивают массу бронхиального секрета. У детей, особенно младшего возраста, кашлевой рефлекс не совершенен, поэтому в момент заболевания ребенок не в состоянии откашливать большое количество мокроты.
С этим связан т.н. эффект заболачивания, или затопления, легких, который быстро развивается и значительно усугубляет состояние ребенка. Следует также учитывать, что максимальное действие таких препаратов обычно заканчивается через 2–3 часа после приема и приходится постоянно добавлять дозу лекарства, что в целом приводит к его передозировке, развитию таких побочных реакций, как тошнота, головокружение, нередко рвота, т.к. рвотный рефлекс у детей, как правило, повышен. К тому же на прием отхаркивающих препаратов, как правило растительного происхождения, часто развиваются аллергические реакции. Эти препараты трудно точно дозировать, что особенно важно в педиатрической практике, в связи с тем что их невозможно стандартизировать. Необходимо также иметь в виду, что каждое растительное вещество имеет системный эффект и, назначая его только «от кашля», можно получить, например, «лекарство от запоров». К тому же препараты растительного происхождения обычно содержат не одно вещество, а сборы, поэтому невозможно предугадать последствия их взаимодействия в организме ребенка. Получается, что простые на первый взгляд растительные лекарственные средства обладают довольно сложными медицинскими особенностями их применения. Однако, как показывает практика, препараты именно данной группы, к сожалению, необоснованно пользуются популярностью среди родителей, которые часто самостоятельно их назначают, что абсолютно недопустимо.
Действие муколитических средств направлено на разжижжение мокроты, и в отличие от отхаркивающих они не увеличивают ее объем. Следует также отметить, что муколитики нельзя назначать вместе с отхаркивающими и противокашлевыми средствами, т.к. они обладают взаимоисключающим лечебным действием. Муколитики – это группа лекарственных препаратов, которая тоже делится на подгруппы в зависимости от происхождения, различного химического строения, имеет разные точки приложения, механизмы действия и разные лечебные эффекты. Они повышают текучесть мокроты, нормализуют ее биохимический состав, улучшают отхождение за счет увеличения мукоцилиарного клиренса, могут влиять на бокаловидные клетки слизистой бронхов, снижая повышенную секрецию. У муколитиков довольно широкие показания к применению: наличие вязкой, труднооткашливаемой слизистой, слизисто-гнойной или гнойной мокроты; трахеиты, острые и хронические бронхиты, бронхиолиты, пневмонии, хроническая обструктивная болезнь легких, бронхоэктатическая болезнь у взрослых; муковисцидоз; ателектазы в результате мукоидной закупорки бронхов; наличие трахеостомы; в качестве профилактических средств против осложнений после операций на органах дыхания, после эндотрахеального наркоза; риносинуситы и т.д.
К муколитикам с прямым типом действия относятся вещества неферментного происхождения, разрушающие сложные химические соединения (ферменты и полисахариды), разрывая дисульфидные связи между белковыми молекулами мокроты, – это тиолы, ацетилцистеин и др. Эти препараты содержат тиольную группу, которая делает мокроту менее вязкой, что и способствует более легкому удалению ее из бронхиального дерева. Основной представитель этой группы – N-ацетилцистеин. Он является производным L-цистеина и в составе молекулы содержит реактивные свободные сульфгидрильные группы (SH), обеспечивающие прямое муколитическое действие за счет разрушения дисульфидных связей кислых мукополисахаридов бронхиальной слизи. В результате происходит деполимеризация макромолекул мукопротеидов и бронхиальная слизь становится менее вязкой и адгезивной. Ацетилцистеин помимо муколитической активности служит мощным прямым и непрямым антиоксидантом: уменьшает процессы перекисного окисления липидов, сохраняет целостность клеточных стенок. Свободные радикалы усиливают развитие острого или хронического воспаления в дыхательных путях, вызывая деструкцию легочной ткани. Прямое антиоксидантное действие связано с тем, что свободная сульфгидрильная группа молекулы ацетилцистеина взаимодействует с электрофильными группами свободных радикалов и реактивных кислородных метаболитов, нейтрализуя их действие. К прямому антиоксидантному действию также относится защита α1-антипротеина. Непрямое антиоксидантное действие связано с тем, что ацетилцистеин является предшественником глутатиона, который в свою очередь принимает участие в процессах детоксикации организма, защиты слизистых дыхательных путей от внешних и внутренних повреждающих воздействий. Ацетилцистеин способен также снижать возможность микроорганизмов колонизироваться на поверхности слизистой дыхательных путей, проявляя спарринг-эффект с антибиотиками (т.н. вторичный антибактериальный эффект). При пероральном приеме ацетилцистеин хорошо всасывается из желудочно-кишечного тракта. Максимальная концентрация в плазме крови достигается уже через час после введения, распределяется во всем организме равномерно, при этом в тканях (в т.ч. в дыхательных путях) и плазме крови отмечается значительное возрастание количества сульфгидрильных групп. Некоторые протеолитические ферменты являются также муколитиками прямого типа действия (дорназа альфа, трипсин, химотрипсин, рибонуклеаза, дезоксирибонуклеаза, альфа-химотрипсин, стрептокиназа). Они способны разрушать пептидные связи в молекуле белка, расщеплять высокомолекулярные продукты распада белков (полипептиды) или нуклеиновые кислоты (ДНК и РНК). Важно отметить, что единственным ферментом, разрешенным сегодня к практике с муколитической целью в виде специального раствора для небулайзерной терапии, остается дорназа альфа, который применяется в базисной терапии пациентов с муковисцидозом. Другие препараты сегодня не применяются, т.к. муколитический эффект их очень мал, а осложнений довольно много (повреждение слизистой оболочки дыхательных путей, кровохаркание, бронхоспазм, аллергические реакции, усиление деструкции межальвеолярных перегородок, например, при дефиците альфа-антитрипсина, а также побочные эффекты со стороны других органов).
Группа муколитиков непрямого типа действия довольно разнообразна. Это препараты, изменяющие адгезивность гелевого слоя (бромгексин, амброксол, бикарбонат натрия, этансульфат натрия); препараты, снижающие выработку слизи и изменяющие ее состав (S-карбоксиметилцистеин, летостеин, собрерол); пинены и терпены (камфора, ментол, терпинеол, эфирные масла); препараты, снижающие выработку слизи железами бронхов (β2-адреномиметики, глюкокортикоиды, М-холиноблокаторы); препараты, действующие рефлекторно на мышцы бронхов (цитрат натрия, хлорид аммония, ипекакуана, термопсис), сегодня практически не используются на практике. Эти препараты иногда называют мукокинетиками.
Действие карбоцистеина происходит за счет другого механизма. Он активирует сиаловую трансферазу – фермент бокаловидных клеток слизистой оболочки бронхов. Это приводит к нормализации количественного соотношения кислых и нейтральных сиаломуцинов мокроты: уменьшает количество нейтральных гликопептидов и увеличивает количество гидроксисиалогликопептидов, восстанавливает вязкость и эластичность. Нормализуется структура и регенерация слизистой оболочки, до нормального соотношения уменьшается количество бокаловидных клеток, снижается количество слизи, улучшается мукоцилиарный транспорт. После перорального приема карбоцистеина максимальная концентрация в сыворотке крови и слизистой оболочке дыхательных путей создается через 2 часа и поддерживается в течение 8 часов. Карбоцистеин показан при остром и хроническом бронхите, например, на фоне муковисцидоза. Необходимо помнить, что неферментные муколитики противопоказаны при легочном кровотечении, язвенной болезни желудка и двенадцатиперстной кишки, могут вызывать диспепсические явления (тошноту, изжогу, рвоту, боли в животе, диарею и запоры), гиперсаливацию или сухость во рту, ринорею и аллергические реакции.
Ярким представителем неферментных муколитиков непрямого типа действия является амброксола гидрохлорид. За последние три десятилетия амброксол широко применяется в качестве мукорегуляторного агента в разных формах – как в виде монотерапии, так и в сочетании с антибактериальными препаратами. Молекула амброксола обладает несколькими механизмами действия, что обусловливает ее сложную фармакологию. В дополнение к хорошо известному свойству очищать бронхи от мокроты амброксол, как было показано, обладает и антиоксидантными, противовоспалительными, анальгезирующими, анестестезирующими, противовирусными, а также антибактериальными свойствами [1–5]. Амброксол применяется в качестве муколитической терапии при острых и хронических заболеваниях бронхолегочной системы, ассоциированных с усилением продукции и нарушением формирования и отделения мокроты. Усиление секреции жидкости и мукоцилиарного клиренса способствует откашливанию [6]. В некоторых зарубежных публикациях описаны дополнительные свойства этой молекулы, несомненно имеющие практическое значение в терапии. Описан местный анестетический эффект амброксола, наблюдаемый на модели глаза кроликов, он расценивается как блокатор натриевого канала [7]. In vitro-исследования показали, что амброксол блокирует клонированный нейрональный натриевый канал, и это связывание является обратимым и зависимым от концентрации вещества в сыворотке [8]. Было показано, что амброксол in vitro также значительно сокращает высвобождение цитокинов из крови [9]. Эти фармакологические свойства согласуются с наблюдениями в клинических исследованиях по изучению эффективности терапии амброксолом патологии верхних дыхательных путей, при этом отмечено ослабление боли и дискомфорта, связанного с болью, локализующейся в области уха, носа и трахеи [10]. Амброксол часто комбинируется с приемом антибиотиков (амоксициллина), поскольку увеличивает концентрацию антибиотиков в мокроте [11]. Вследствие упомянутых выше свойств амброксол в настоящее время применяется при патологиях, сопровождающихся гиперсекрецией слизи, таких как трахеобронхит, эмфизема с бронхитом, хронические воспалительные заболевания дыхательных путей, бронхоэктазы и бронхиальная астма [6]. Сегодня опубликован ряд данных, свидетельствующих о роли амброксола при некоторых болезнях дыхательных путей, сопровождающихся развитием бактериальных пленок.
Бактериальные пленки – это колонии бактерий, прикрепленных к органической или неорганической поверхности, вырастающих в самопродуцируемый экстрацеллюлярный матрикс, содержащий ДНК-а, протеины и полисахариды [12]. Поскольку в этих колониях микроорганизмы растут структурируемым сообществом, бактериальная пленка служит организованным выражением примера своего рода бактериального «социального» поведения [13]. Поэтому неудивительно, что процесс формирования бактериальных пленок сильно регулируется специфическими механизмами, среди которых наиболее важным остается quorum sensing [14]. Термин «quorum sensing» относится к группе регуляторных систем, посредством которых бактериальные популяции «ощущают» клеточную плотность колонии и запускают адаптивные ответы на изменения собственной плотности [15]. Важно для практики врача помнить, что бактериальные пленки могут формироваться на медицинских предметах, таких как внутривенный катетер, мочевой катетер, эндотрахеальная трубка. Поэтому они играют большую роль в возникновении инфекции, особенно для тяжелых пациентов [16].
К ранее известным противовоспалительным и мукокинетическим свойствам амброксола, продемонстрированным много лет назад, приводится несколько аргументов, свидетельствующих о пользе амброксола для профилактики и лечения инфекций. Так, было показано, что молекула амброксола также обладает специфической активностью в отношении бактериальных пленок и способностью улучшать мукоцилиарный клиренс. Недавние исследования показали, что амброксол разрушает структурную целостность бактериальной пленки; в частности, это было показано в работе с изолятами Pseudomonas aeruginosa [17]. Ингибиторный эффект амброксола не ограничивается только бактериями: есть указания на его действие в отношении грибов. В ряде исследований было продемонстрировано, что амброксол вмешивается в процесс приобретения резистентости изолятами Candida parapsilosis [18].
В отличие, например, от ацетилцистеина амброксол не является истинным муколитическим препаратом. Традиционно он рассматривается как мукокинетик. Идея, что амброксол воздействует на вязкость слизи не только путем прямого влияния на белки мокроты, но и посредством вмешательства в транспорт ионов вдоль поверхности эпителия мембраны, предполагалась и ранее [19]. Несмотря на то что на сегодняшний день пока нет контролируемых клинических исследований, направленных на оценку эффекта амброксола у пациентов отделения реанимации с вентилятор-ассоциированной пневмонией, результаты ряда работ в этом направлении обнадеживают. В частности, прием 990 мг амброксола в день, растворенных в 500 мл изотонического раствора и введенных внутривенно в течение 4–6 часов, позволил сократить возникновение постоперационной пневмонии и гипоксемии у пациентов с травмой спинного мозга после оперативного лечения [20]. Амброксол оказывает благоприятный эффект на пациентов после проведения кардиопульмонального шунтирования – состояния, при котором имеет место системное воспаление [21]. Имеются работы, показывающие положительный эффект приема амброксола пациентами с резекцией легких [22]. Описаны отдельные, хотя и обладающие низким уровнем доказательности, работы об эффективности применения амброксола при кистозном фиброзе и обострении хронической обструктивной болезни легких [23, 24].
Амброксол успешно назначается в терапии болезней органов дыхания различной этиологии у детей и взрослых уже более 35 лет [25–27]. Молекула амброксола гидрохлорида – точная копия природной молекулы. В XIII в. на территории Шри-Ланки и Индии, на острове Ява было известно растение – кустарник, который сегодня имеет название Adhatoda vasica (Адатода сосудистая). Уже в те далекие времена лечебные свойства этого растения использовали при лечении нервных болезней (невралгии) и при заболеваниях органов дыхания (бронхите, кашле, коклюше, астме), а также при дизентерии, диарее, ознобе, ревматизме и воспалении кожи. Указанное «лекарство» получали из сока листьев растения, цветов, фруктов, корней, использовалось его отхаркивающее, антиспазматическое, успокоительное и глистогонное действия. Активным экстрактом этого растения считаются алкалоиды – т.н. вазициноиды (вазицин и вазицинон), которые обладают подобным эуфиллину действием и имеют в своем составе эфирное масло [28].
Основные свойства амброксола: высокий муколитический и выраженный отхаркивающий эффекты, а также дополнительные (антиоксидантное, противоспалительное) свойства стимулировать синтез сурфактанта и оказывать повреждающее действие на биопленки бактерий, улучшать местный иммунитет [29]. При непродуктивном кашле он облегчает боль в груди и частично смягчает кашлевой рефлекс. Педиатру важно знать, что амброксол проникает через плаценту в цереброспинальную жидкость и в грудное молоко, но имеет высокий уровень безопасности. Частота побочных эффектов, например диареи и тошноты, при его применении в лекарственной форме сиропа у детей с острыми и хроническими заболеваниями дыхательных путей составила 0,46%. При необходимости может назначаться беременным во 2-м и 3-м триместрах. При угрозе преждевременных родов амброксол применяется для профилактики дистресс-синдрома с 28-й недели беременности и в отношении недоношенных – также при угрозе дистресс-синдрома [30, 31].
В научных исследованиях было убедительно показано положительное взаимодействие амброксола с антибиотиками. Он способствует повышению эффективности антибиотика, увеличивая его концентрацию в бронхиальном секрете [32]. При совместном использовании амброксола и антибиотика увеличивается скорость пассивной диффузии антибиотиков из плазмы крови в легочную ткань без изменений концентраций антибиотиков в плазме крови [33]. Дальнейшие наблюдения показали, что амброксол улучшает бионакопление антибиотиков в бронхоальвеолярной жидкости больных хроническими заболеваниями легких [34].
В педиатрическом сообществе и сегодня продолжаются активные обсуждения по сравнению двух препаратов – амброксола и бромгексина. Сразу следует сказать, что эти препараты обладают сходными свойствами, но в отличие от бромгексина именно амброксол превосходит его по силе лечебного эффекта и клинической эффективности, т.к. является активным его метаболитом. Действие амброксола начинается быстро – уже через 30 минут. Терапевтическое действие бромгексина проявляется к 4–6-му дню терапии. Препараты имеют разную биодоступность: у амброксола – высокая (75%), у бромгекисна – низкая (25%). После начала курса перорального приема амброксола его максимальный эффект появляется на 3-й день лечения. При лечении хронических заболеваний за 2 недели терапии количество мокроты и ее вязкость уменьшаются наполовину.
Важно помнить, что в целом все муколитики противопоказаны в 1-м триместре беременности и при кормлении грудью. Больным бронхиальной астмой с целью профилактики рефлекторного бронхоспазма перед ингаляционным введением муколитиков следует применять ингаляционный β2-адреномиметик. Всегда следует учитывать возможные эффекты при сочетании муколитиков с другими часто применяемыми лекарственными средствами (см. таблицу).
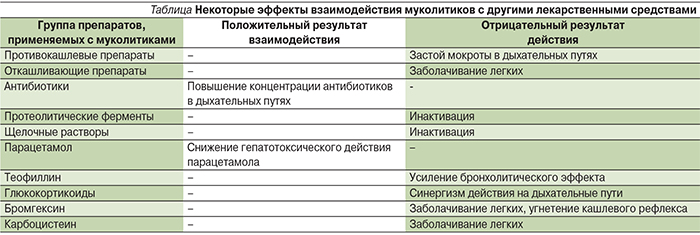
Таким образом, группа препаратов, которые влияют на кашель и изменяют свойства мокроты при острых и хронических заболеваниях дыхательных путей, довольно большая и разнообразная. И каждое лекарственное средство имеет свою точку приложения. Амброксол показал свою эффективность и безопасность в отношении детей при лечении различной респираторной патологии. Разнообразие лекарственных форм амброксола делает его особенно удобным к применению в педиатрической практике.



