Аллергические болезни (АБ) – частая причина нарушения состояния здоровья детей. По данным эпидемиологических исследований, аллергические реакции и АБ выявляются среди 20–50 % детского населения. Патогенетическую основу АБ составляет иммунное воспаление, возникающее под воздействием аллергенов вследствие нарушения регуляции иммунного ответа, наследственного предрасположения к аллергии [1], изменения барьерной функции органов и тканей [2]. Аллергия рассматривается как реакция организма на поступление аллергена в его внутренние среды [3]. В связи с этим в лечении АБ большое значение придается элиминации специфических триггерных факторов и применению иммунологических методов нивелирования воздействия причиннозначимых аллергенов [4].
Аллерген-специфическая иммунотерапия (АСИТ) – в настоящее время единственный метод лечения, оказывающий влияние на естественное течение АБ с достижением стойкой клинической ремиссии. АСИТ считается наиболее эффективным способом лечения АБ как у детей, так и у взрослых [5–9].
Метод АСИТ представляет собой введение в организм больного лечебных аллергенов (аллерговакцин) в возрастающих дозах до уровня, при котором возможно уменьшение проявлений болезни при последующей экспозиции с аллергеном.
Лечебные аллергены, применяемые для АСИТ
Для проведения АСИТ используют следующие группы лечебных аллергенов:
- водно-солевые экстракты аллергенов;
- модифицированные лечебные;
- сублингвальные (САГ);
- пероральные.
АСИТ проводится преимущественно водно-солевыми экстрактами причиннозначимых аллергенов, которые помимо аллергенных белков могут содержать другие примеси белкового и небелкового происхождения. Очищенные аллергены характеризуются высокой степенью антигенной стандартности, стабильности и активности на единицу массы, в связи с чем они обладают повышенной иммунологической безопасностью.
Модифицированные аллергены обладают более благоприятным профилем безопасности и выраженной иммуногенной активностью. В аллергологической практике для проведения АСИТ широко используются аллергоиды и депонированные лечебные аллергены.
За последние годы для проведения АСИТ стали чаще применяться САГ, выпускаемые в виде растворов и дозируемые каплями. Стандартизация САГ производится в тех же единицах, что и лечебных аллергенов для подкожного введения, но дозы САГ во много раз выше, чем при подкожном введении. Существуют быстрорастворимые формы САГ в виде таблеток для однократного приема. В России для проведения АСИТ используются водносолевые экстракты аллергенов, пыльцевые аллергоиды, САГ производства Sevapharma (Чехия), сорбированный на фосфате кальция пыльцевой аллерген – препарат Фосталь (Франция).
Механизмы АСИТ
АСИТ проводится при IgE-опосредуемых АБ: атопической бронхиальной астме (БА), персистирующем (круглогодичном) аллергическом рините (АР), интермиттирующем (сезонном) АР, поллинозах, дермореспираторном синдроме, инсектной аллергии.
Развитие указанных заболеваний в значительной мере связано со снижением контроля регуляторными Т-клетками (CD4+CD25+FOXP3 Treg, Tr1, Th3) гиперактивации иммунной системы [10]. Под влиянием АСИТ отмечается усиление регуляторной функции Tr1, Th3, CD4+CD25+Treg, проявляемое повышением продукции интерлейкина-10 (ИЛ-10), трансформирующего фактора роста β (TФР-β), уменьшением пролиферации аллерген-специфических Т-лимфоцитов, супрессией IgE-ответа, формированием аллерген-специфической толерантности. При проведении АСИТ под воздействием интенсивной антигенной стимуляции происходит перестройка иммунного ответа на новый тип, характеризуемый увеличением продукции интерферона γ (ИФН-γ) и ИЛ-10 Т-клетками, повышением содержания CD4+CD25+FOXP3+Т-клеток, числа клеток, продуцирующих ИЛ-12, что свидетельствует о переключении Th2-цитокинового профиля на Th1-цитокиновый профиль [11]. Под воздействием АСИТ клещевыми и пыльцевыми аллергенами у детей с БА отмечается повышение продукции ИЛ-10, ИЛ-2, ИФН-γ и снижение уровня провоспалительных цитокинов (ИЛ-1, фактор некроза опухоли α, ИЛ-6, ИЛ-8) в сыворотке крови [12]. Снижение активности Th2-лимфоцитов на фоне АСИТ проявлялось в снижении продукции ИЛ-4. Под влиянием АСИТ наблюдается усиление экспрессии рецепторов для ИЛ-2, что способствует уменьшению дисбаланса Th1/Th2-лимфоцитов. При позитивном результате АСИТ у детей с БА обнаружено снижение уровня Е-селектина, молекулы межклеточной адгезии ICAM-1 и хемокина RANTES [12], способствующее уменьшению аллергического воспаления бронхов.
Положительный результат АСИТ сопровождается увеличением продукции IgG-антител, повышением уровня IgG и IgA в секретах, супрессией сезонного повышения уровня специфических IgE-антител к пыльцевым аллергенам при поллинозах, сменяющейся при длительной АСИТ снижением их продукции, уменьшением количества медиаторов, высвобождаемых тучными клетками и базофилами при экспозиции с причиннозначимыми аллергенами, восстановлением баланса между Т-хелперами и Т-супрессорами [2, 4]. Содержание специфических IgG в сыворотке крови достигает максимума после 2 лет АСИТ и в последующем не претерпевает существенных изменений. Повышение содержания IgG в сыворотке крови под влиянием АСИТ происходит в основном за счет субкласса IgG4 и в меньшей степени – субкласса IgG1; при проведении АСИТ аллергеном Cladosporium herbarum IgG-ответ включает также повышение уровней IgG2 и IgG3 [13].
При АСИТ изменяется и продукция специфических IgE-антител. После первого ее курса аллергенами плесневых грибов Dermatophagoides pteronyssinus наблюдается повышение продукции специфических IgE-антител, при продолжении ее в течение нескольких лет отмечается постепенное снижение уровня общего и специфических IgE в сыворотке крови до значений нормы [7]. У детей с поллинозом проведенная до начала сезона цветения причинно-значимых растений АСИТ тормозит сезонный прирост продукции специфических IgE-антител [9]. Повышение уровня специфических IgG4-антител обычно представляет собой позднюю реакцию на высокую концентрацию вводимого аллергена.
АСИТ может избирательно стимулировать аллергенспецифический IgA2-ответ, продукцию ИЛ-10 и TФР-β, тем самым способствуя развитию толерантности к причиннозначимым аллергенам [14].
Результатом изменения характера реагирования на аллерген после успешно проведенной АСИТ является снижение тканевой (органной) чувствительности при воздействии на организм аллергена, снижение неспецифической тканевой гиперреактивности, ингибирование морфологических и функциональных признаков аллергического воспаления.
Показания к АСИТ
К основным показаниям к проведению АСИТ относится невозможность прекращения контакта с причиннозначимыми аллергенами, прежде всего c такими, как аллергены домашней пыли, микроклещей домашней пыли, пыльцевые аллергены, аллергены некоторых плесневых грибов. АСИТ проводится больным инсектной аллергией, проявляемой системными аллергическими реакциями, чаще всего возникающими у таких пациентов при укусах пчелами и осами.
АСИТ сравнительно редко проводится при пищевой аллергии. Имеются сообщения об эффективности ее проведения аллергенами коровьего молока, куриных яиц детям раннего возра-ста, страдающим гастроинтестинальной пищевой аллергией и атопическим дерматитом [15]. В то же время другие исследователи отмечают низкую эффективность АСИТ при пищевой аллергии у детей [16]. Проведение парентеральной АСИТ подростков с сочетанными проявлениями поллиноза и пищевой аллергии к продуктам, имеющим перекрестную аллергическую реактивность с пыльцевыми антигенами, оказывается эффективной для 80 % больных поллинозом и для 52 % – с пищевой аллергией.
Имеются сообщения об эффективности АСИТ детей при БА, ассоциированной с бактериальной сенсибилизацией, подтвержденной обнаружением в сыворотке крови специфических IgE к бактериальным аллергенам, при этом отмечено позитивное влияние АСИТ на течение болезни у 82 % больных [17].
АСИТ детей при АБ может проводиться только при четком подтверждении причиннозначимой роли аллергенов в патогенезе болезни и установлении IgE-опосредуемого механизма ее развития. Европейская ассоциация аллергологов и клинических иммунологов рекомендует начинать АСИТ детям с 5 лет и старше; больным младше 5 лет АСИТ проводится по поводу тяжелой инсектной аллергии.
Больным БА АСИТ должна проводиться и при хорошем ответе на фармакотерапию, поскольку только специфическая иммунотерапия способствует достижению ремиссии признаков болезни и видоизменению ее течения за счет достижения аллергенспецифической толерантности.
Противопоказания к АСИТ
АСИТ не проводится при обострении АБ, при их сочетанных проявлениях с иммунодефицитами, тяжелых заболеваниях сердечно-сосудистой системы, воспалительных заболеваниях печени, почек, поджелудочной железы. Противопоказанием к проведению АСИТ служит также наличие аутоиммунных заболеваний, острых инфекционных болезней. АСИТ противопоказана больным, получающим лечение β-адреноблокаторами. АСИТ не может проводиться детям с неконтролируемой или частично контролируемой БА.
Методы проведения АСИТ
Выбор аллергена для проведения АСИТ основывается на оценке данных аллергологического анамнеза, результатов кожного тестирования, аллергодиагностики in vitro, при необходимости – провокационных назальных и конъюнктивальных тестов с аллергенами.
В настоящее время используются инъекционные и неинъекционные методы проведения АСИТ.
Инъекционный способ проведения АСИТ состоит в подкожном введении аллергенов в нижнюю треть плеча.
К неинъекционным методам АСИТ относятся следующие способы ее проведения:
- пероральный метод, предусматривающий одномоментное проглатывание аллергена в каплях, таблетках или капсулах;
- сублингвальный метод, при котором аллерген удерживается под языком в течение 1–2 минут и затем проглатывается или выплевывается;
- интраназальный метод, при котором водная или порошкообразная форма аллергена вводится в нос при помощи пипетки или специального устройства.
В зависимости от длительности курсового лечения выделяют круглогодичную, предсезонную и сезонную АСИТ. При выявлении причиннозначимой бытовой сенсибилизации проводят круглогодичную специфическую иммунотерапию. При поллинозе осуществляется предсезонная АСИТ.
Лечебную смесь аллергенов для иммунотерапии готовят с учетом выраженности выявляемой к ним чувствительности, выбирая при этом главные, клинически значимые аллергены. Не рекомендуется смешивать неродственные аллергены, поскольку они обладают взаимно подавляющей активностью (пыльцевые аллергены теряют свою активность при смешивании с аллергенами клещей домашней пыли, плесеней, тараканов) [2].
Начальную дозу лечебных аллергенов подбирают путем аллергометрического титрования с использованием prick-теста или внутрикожного теста с последующим началом АСИТ с разведения аллергенов, вызвавших сомнительную или слабоположительную реакцию. Чаще всего АСИТ начинают с введения аллергенов в разведении 1 : 1000000 (10ˉ⁶).
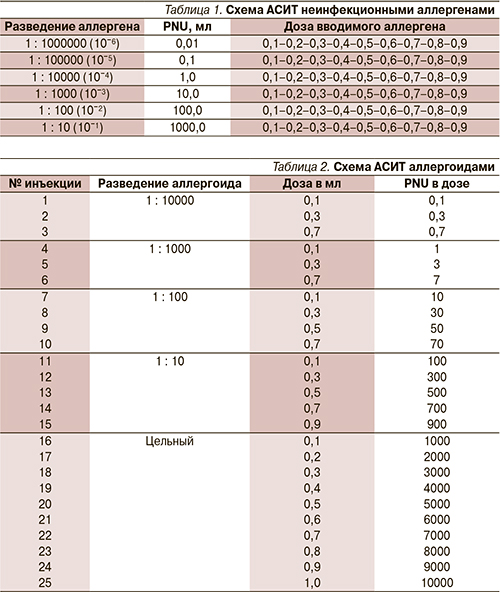
Парентеральный способ терапии является основным методом АСИТ. При данном методе иммунотерапии осуществляют постепенное наращивание дозы вводимого аллергена до достижения максимальной терапевтической дозы и в последующем проводят поддерживающую терапию. На этапе достижения максимальной терапевтической дозы лечебные аллергены в концентрации 10ˉ⁶ (0,01 PNU в 1 мл) по 10ˉ⁴ (1 PNU в 1 мл) вводят подкожно ежедневно или через день, затем с интервалом 7–10 дней до достижения поддерживающей дозы, которую вводят с интервалом 14 дней. АСИТ больных поллинозами детей заканчивают за 2 недели до начала сезона цветения причиннозначимых растений. В табл. 1 приведена примерная схема АСИТ неинфекционными аллергенами.
За последние годы в аллергологической практике стала шире использоваться ускоренная схема проведения АСИТ [18]. Ее применяют в случаях, когда возникает необходимость в сокращении сроков лечения и ускорении достижения поддерживающей дозы лечебных аллергенов для продолжения лечения. При проведении парентеральной АСИТ по ускоренной схеме аллергены вводят подкожно от 2 до 3 раз в день, лечение проводится в аллергологическом отделении.
Парентеральная АСИТ может проводиться модифицированными аллергенами. Аллергоиды характеризуются уменьшенной аллергенностью и значительной иммуногенностью. Применение их позволяет повышать эффективность лечения за счет введения большей суммарной дозы лечебных аллергенов и меньшей частоты развития побочных явлений. В табл. 2 приведена схема АСИТ отечественными аллергоидами из пыльцы деревьев, злаковых трав, полыни, домашней пыли. Первые подкожные инъекции аллергоидов проводятся ежедневно или через день. При введении аллергоидов в разведении 1 : 100 интервал между инъекциями увеличивается и составляет 3 дня. При иммунотерапии аллергоидами подкожно может вводиться цельный аллергоид с интервалом в 7 дней.
К пролонгированным формам лечебных аллергенов относится препарат Фосталь, содержащий ультрафильтрованный экстракт смеси пыльцы деревьев (ольха, береза, граб, орешник обыкновенный), адсорбированный на суспензии фосфата кальция. Содержание активного вещества в препарате выражается индексом реактивности (ИР/мл), определяемым с использованием экстракта аллергена 100 ИР/мл при кожном тестировании.
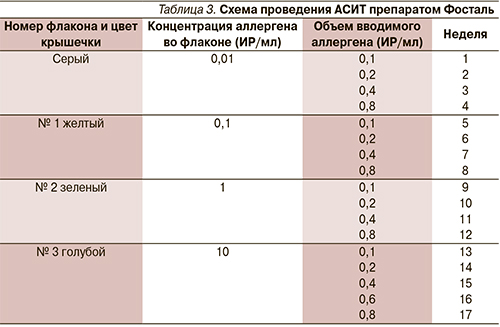
Для достижения максимальной терапевтической дозы осуществляется постоянное увеличение подкожно вводимой дозы аллергена с минимальной концентрацией 0,01 ИР/мл до максимальной 10 ИР/мл (табл. 3).
Для проведения поддерживающей терапии препарат вводится в концентрации 10 ИР/мл в объеме 0,8 мл. Первые две поддерживающие инъекции препарата Фосталь вводятся с интервалом 15 дней, затем 1 раз в месяц или реже, но интервал между инъекциями не должен превышать 6 недель. Иммунотерапия поддерживающей дозой этого препарата проводится в течение 3–5 лет. АСИТ препаратом Фосталь достаточно эффективна для больных поллинозом [19].
За последние годы в лечении детей с атопическими болезнями широкое применение находит сублингвальная АСИТ. Терапевтическую эффективность ее связывают с взаимодействием высоких доз лечебного аллергена с мукозальной иммунной системой, приводящим к формированию аллерген-специфической толерантности [20]. Сублингвальная АСИТ вызывает увеличение числа CD4+CD25+Foxp3+ клеток в слизистой оболочке полости рта, сопровождающееся повышением содержания в сыворотке крови аллерген-специфических IgG1 и IgG4, а также возрастанием в сезон цветения растений уровней IgA1 и IgA2 [21]. Установлено, что под влиянием сублингвальной АСИТ при поллинозах после 2 лет лечения отмечается возрастание уровней аллерген-специфических IgE, IgG, IgG4, IgA, а также TФР-β, при этом выявляется связь между повышением содержания IgA и TФР-β после первого и второго курсов иммунотерапии [22].
В настоящее время в России сублингвальная АСИТ проводится детям в основном стандартизированными аллергенами: весенняя смесь ранняя (аллергены пыльцы деревьев), смесь трав (аллергены пыльцы луговых трав), осенняя смесь пыльцевая (аллергены пыльцы сорных трав) и смесь плесеней наружных (грибковые аллергены) фирмы Sevapharma (Чехия).
Содержание активного вещества в указанных аллергенах выражено в биологических единицах JSK (единица стандартного качества), соответствующих PNU. Аллергены выпускаются во флаконах с различной концентрацией: 0,1; 1; 10; 100; 1000 и 10000 JSK/мл (PNU/мл). АСИТ проводится в два этапа: фаза инициации (она характеризуется постепенным повышением доз и концентрации до предельно допустимой дозы) и фаза поддержания, которая характеризуется многократной подачей максимально допустимой дозы. Начиная с 1 капли минимальной концентрации (0,1 JSK) каждый последующий прием доза повышается на 1 каплю вплоть до дозы 10 капель. В последующем переходят на более высокую концентрацию и опять повышают дозу от 1 до 10 капель. По достижении наивысшей концентрации максимальное количество (10 капель в сутки) назначают 3 раза в неделю. Кратность назначения препарата корректируется в соответствии с переносимостью препарата и состоянием больного. Сублингвальная АСИТ может проводиться как круглогодично, так и в предсезонный период.
Эффективность АСИТ
АСИТ видоизменяет характер реагирования иммунной системы на аллерген и влияет на естественное течение АБ. Под ее воздействием отмечается снижение органной и тканевой чувствительности к причиннозначимым аллергенам; проведение ее способствует достижению длительной и стойкой ремиссии АБ, уменьшению потребности в противоаллергических препаратах. АСИТ более эффективна на раннем этапе болезни, она предупреждает расширение спектра сенсибилизации, лечебное действие АСИТ достигается в полной мере после повторных (3–5) курсов лечения. Наиболее часто АСИТ проводится детям с атопической БА, поллинозами, АР.
Достаточно эффективна АСИТ при атопической БА [23–25, 28]. При проведении ее аллергенами домашней пыли, Dermatophagoides pteronyssinus парентеральным, сублингвальным и интраназальным способом положительный результат лечения достигается в отношении 86, 82 и 87 % больных соответственно [12]. Среди детей с легким течением БА положительный результат отмечается в 86,0 %, при среднетяжелом – в 81,5 % случаев. При тяжелой БА АСИТ проводилась при достижении контроля за течением болезни в результате проведения базисной (противовоспалительной) терапии. Положительный результат АСИТ у детей с тяжелой БА обеспечивался реже, чем при легкой и средне-тяжелой, – в 65,4 % случаев.
Более эффективна АСИТ при БА у детей с моновалентной, чем с поливалентной, сенсибилизацией (соответственно у 82,4 и 71,7 %). Эффективность неинвазивной АСИТ при БА была выше у детей в возрасте 3–5 лет (86,2 % положительных результатов) по сравнению с детьми старшего возраста (77 %).
Для проведения АСИТ у больных БА также используются аллергены плесневых грибов: лечение ими проводится после подтверждения IgE-опосредуемого механизма болезни и этиологической значимости в развитии сенсибилизации к этим аллергенам.
При БА, обусловленной сенсибилизацией к аллергенам домашних животных (кошки, собаки), при отказе родителей устранить их из жилого помещения, достаточно эффективной может быть АСИТ эпидермальными аллергенами. После 3-летнего курса АСИТ вакциной, приготовленной из перхоти кошки, толерантность к этим животным сохранялась у больных астмой в течение 5 лет после ее завершения [26].
Атопическая БА у 63 % детей сопровождается сопутствующим круглогодичным (персистирующим) АР. После проведения АСИТ у 80 % этих больных было отмечено уменьшение симптомов АР, улучшение назальной проходимости и достижение устойчивой ремиссии болезни [4, 6]. Проведение АСИТ при АР может предотвратить развитие БА у детей.
АСИТ является наиболее эффективным методом лечения поллинозов. Наиболее эффективна при поллинозах у детей парентеральная АСИТ. После первого года лечения положительный результат отмечается у 92,7 % больных, с увеличением продолжительности иммунотерапии до 2–3 лет увеличивается и число ее отличных и хороших результатов [4].
При поллинозах для детей и подростков эффективна сублингвальная АСИТ, проведение которой позволяет достигать ремиссии болезни или уменьшения проявлений ее у 85,7 % пациентов [27]. Значительное уменьшение симптомов поллиноза чаще отмечается среди больных, получивших при сублингвальной АСИТ более высокую суммарную дозу причиннозначимых пыльцевых аллергенов [28]. Парентеральная АСИТ высокоэффективна при сезонном (интермиттирующем) аллергическом конъюнктивите, обусловленном пыльцевой сенсибилизацией [29]. При поллинозах у детей интраназальная АСИТ позволяет 71,9 % больных добиваться отличных и хороших результатов [30]. Достаточно эффективна при поллинозах у детей интраназальная АСИТ пыльцевыми аллергоидами [8, 31, 32] и пероральными аллергенами [8, 33, 34].
Укусы перепончатокрылых насекомых (ос, пчел, шмелей, шершней) служат одной из наиболее частых причин развития системных аллергических реакций, проявляемых крапивницей, ангиоотеками кожи, подкожной клетчатки, слизистых оболочек, бронхоспазмом, спазмом гладкой мускулатуры желудочно-кишечного тракта, проявлениями сердечно-сосудистой недостаточности, а у отдельных больных и анафилактического шока.
АСИТ аллерговакцинами из ядов насекомых проводится без возрастных ограничений детям, в анамнезе которых присутствуют указания на тяжелые системные аллергические реакции на укусы насекомых и положительные кожные реакции на инсектные аллергены. В настоящее время для проведения АСИТ используют аллерговакцины из яда насекомых. Проводится парентеральная предсезонная АСИТ с начала зимы до конца весны, а на протяжении лета до середины осени вводятся поддерживающие дозы аллерговакцин, продолжительность лечения составляет 3–5 лет, положительные результаты АСИТ аллерговакцинами из ядов насекомых составляют 90–95 %.
Безопасность АСИТ
При проведении парентеральной АСИТ побочные явления в виде крапивницы и бронхоспазма отмечаются у 2,8 % детей с БА [23]. В ходе сублингвальной АСИТ системных реакций отмечено не было. Возникшие при проведении сублингвальной АСИТ побочные реакции у 11 % детей с поллинозом проявлялись обострением АР, атопического дерматита и БА [27].
У 16,7 % детей, получавших сублингвальную АСИТ, и у 28,9 % больных при интраназальной АСИТ были выявлены местные побочные реакции в виде обострения АР, зуда слизистой оболочки губ и щек, исчезавших после назначения антигистаминных препаратов [12]. Частота побочных явлений при проведении АСИТ меньше при использовании высокоочищенных, стандартизированных аллергенов и постепенном наращивании дозы лечебных аллергенов. Тщательное наблюдение за ребенком в ходе иммунотерапии, индивидуальный с учетом состояния больного подход к наращиванию дозы лечебных аллергенов, достижение максимальной дозы вводимых аллергенов и последующее проведение продолжительной поддерживающей терапии – важные условия для достижения оптимального эффекта от АСИТ.



