Всовременных клинических рекомендациях для лечения остеопороза (ОП) в качестве первой линии терапии предложено использовать бисфосфонаты (БФ). Так как лечение ОП направлено на профилактику низкоэнергетических переломов, для достижения максимального результата может потребоваться длительное назначение этих лекарственных средств. Лечение БФ с учетом возраста, анамнеза, наличия переломов, сопутствующих заболеваний может быть рекомендовано больному на 3–5 лет, а в некоторых случаях продлено и до 10 лет.
Длительность использования и стоимость самих препаратов для лечения ОП, особенно созданных на основе современных высоких технологий, влияют на увеличение расходов как со стороны государства и страховых медицинских компаний на лекарственное обеспечение граждан, так и на повышение затрат самого больного. Было установлено, что даже среди больных с перенесенным переломом вследствие минимальной травмы 26% лиц отказались от лечения ОП из-за стоимости рекомендованной терапии [1]. Поэтому в широкой клинической практике определенным выходом из сложившейся ситуации может быть замена брендовых препаратов на воспроизведенные (генерические), но при условии, что генерические препараты (ГП) должны соответствовать тем же стандартам качества, эффективности и безопасности, которые предъявляются к оригинальным лекарственным средствам, чтобы обеспечивать высокий уровень и качество помощи пациентам с ОП.
Показателем качества лекарственной формы и терапевтической эффективности ГП является его биологическая эквивалентность (биоэквивалентность) оригинальному препарату [2]. Введение данного понятия было связано с тем, что лечебная и профилактическая активность любого лекарственного вещества обусловлена не только его химическим строением и физико-химическими свойствами, но и «вторичными» свойствами, приобретенными в результате направленного технологического вмешательства при изготовлении препарата. Так как ГП помимо той же активной субстанции, что и в оригинальном (патентованном) лекарстве, содержат еще и вспомогательные вещества (неактивные ингредиенты, наполнители, консерванты, красители и др.), которые могут влиять на реакцию организма больного на лечение, для внедрения их в практику требуются доказательства их фармацевтической эквивалентности и биодоступности брендовому препарату.
Фармацевтически эквивалентными считаются препараты, назначаемые одним и тем же путем, содержащие одинаковое количество идентичного действующего вещества (веществ) в одинаковых лекарственных формах, соответствующего требованиям одних и тех же или сопоставимых стандартов. Если различия фармакокинетических кривых между оригинальным и генерическим препаратами не превышают 20%, делается заключение об их биоэквивалентности, что позволяет говорить о равноценности ГП и патентованного фармацевтического продукта. Стоимость ГП значительно ниже, т.к. для их регистрации не требуется проведения экспериментальных и клинических исследований, поскольку терапевтические эффекты их активных ингредиентов известны и соответствую таковым оригинальных препаратов.
В большинстве стран мира отмечена тенденция к увеличению использования ГП. Так, на их долю приходится до 20% фармацевтического рынка США, 30–60% от всех продаваемых лекарственных средств в странах Европы и 64% – в Канаде [3]. Однако существует мнение, согласно которому практикующие врачи по разным причинам предпочитают применять оригинальные лекарственные средства, считая, что по своей эффективности ГП уступают брендовым препаратам и имеют большее число побочных эффектов. Результаты опросов врачей разных стран показали, что отношение медицинских работников к ГП зависит от состояния системы здравоохранения и уровня контроля за качеством лекарственных средств [4]. Например, во Франции из 600 опрошенных врачей общей практики 76% активно назначали пациентам ГП, а в Словении 180 из 200 врачей общей практики считали, что ГП также эффективны, как и оригинальные препараты, но при этом каждый четвертый из них указал, что рекомендовал генерики только при наличии данных дополнительных клинических исследований. Почти половина финских врачей различных специальностей, выписывавших пациентам ГП, считали, что не все эти лекарства эффективны и безопасны, а 34 и 45% семейных врачей, участвовавших в онлайн-опросе в Италии, отметили, что эффективность ГП достаточная или хорошая соответственно, но при этом только 14% из них заявили, что большинство их пациентов получают такие лекарственные средства. В Саудовской Аравии анкетирование 900 врачей выявило, что только 16% из них в любой ситуации отдавали предпочтения назначению ГП, при этом врачи общей практики (47%) это делали чаще, чем работавшие в больницах или ведущие частный прием.
На фармацевтическом рынке России ГП для лечения ОП представлены только среди БФ, и наибольшее их количество зарегистрировано для алендроната (АЛН). Преимущество использования оригинального АЛН заключается в большом опыте его длительного применения как в клинических исследованиях, так и в реальной врачебной практике, доказавших антипереломный эффект для больных ОП, в то время как применение большого числа его генериков обеспечивает существенную выгоду благодаря более низкой цене.
Мы провели независимые опросы врачей и пациентов с целью оценки частоты назначения генериков АЛН для лечения ОП в реальной клинической практике.
Были проанкетированы 307 врачей поликлинического звена здравоохранения, которые консультируют больных ОП в своей повседневной практике. Это были представители шести специальностей: гинекологи, неврологи, ревматологи, терапевты, травматологи (хирурги) и эндокринологи. Установлено, что пациентов с ОП достоверно чаще, чем врачи других специальностей, наблюдали ревматологи и эндокринологи (p<0,001 и <0,05 соответственно). При этом в течение месяца под наблюдением ревматолога было в среднем 20 [12; 40] пациентов с ОП, у эндокринологов – 16 [8; 20], реже такие больные бывали на приеме у травматологов (12 [6; 18]). Гинекологи, неврологи и терапевты принимали в среднем по 6 пациентов с ОП в месяц.
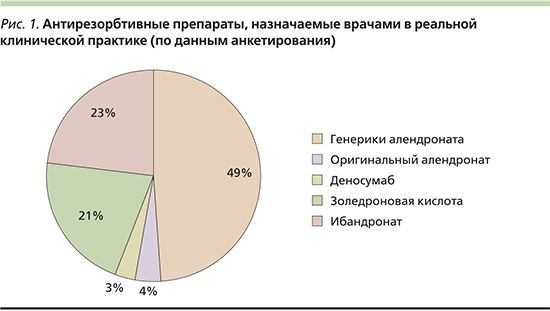
Анализ назначаемой врачами терапии показал, что 24% опрошенных специалистов рекомендовали кальций с витамином D в качестве монотерапии ОП и только в 76% случаев ими назначались патогенетические антиостеопоретические препараты. Среди последних использовались практически все представленные в клинических рекомендациях медикаментозные средства первой и второй линий терапии, но наиболее часто указывались генерики АЛН, на долю которых приходилось 49% от всех назначаемых препаратов для лечения ОП (рис. 1).
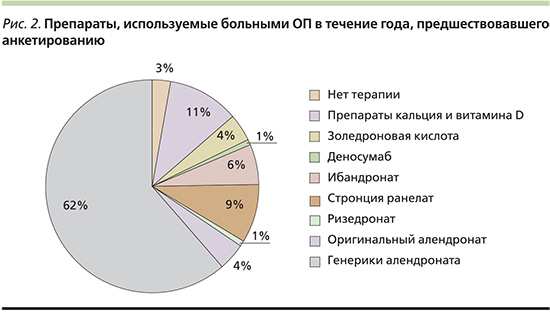
На выбор врачей при назначении терапии по поводу ОП влияли различные факторы. При этом 81% врачей считали, что высокая стоимость лечения может стать причиной отказа больного от приема назначенного лекарства, а 22% отметили и возможные побочные эффекты препаратов. Среди других факторов, способных влиять на приверженность пациента лечению, были отмечены масса других принимаемых препаратов (51%), собственное суждение больных о своем состоянии (40%) и длительность планируемой терапии (38%). Проведенное анкетирование 1799 пациентов с ОП, в т.ч. 1534 (85%) женщин и 265 (15%) мужчин, старше 25 лет (средний возраст – 63,3±8,4 года) с продолжительностью заболевания не менее года (в среднем 2,7±1,8 года), проживающих в разных регионах нашей страны, показало, что лечение АЛН в течение года, предшествовавшего опросу, получали 1172 (65%) человека, из них 1118 (95%) – различными ГП этого лекарственного средства (рис. 2).
Больные, лечившиеся оригинальным и воспроизведенными препаратами АЛН, не различались по возрасту, среди них была одинаковая доля лиц мужского пола, они принимали практически одинаковое общее количество таблеток в день по поводу всех сопутствовавших заболеваний. Уровень образования, длительность заболевания и продолжительность лечения в обеих группах также не различались. Но оказалось, что в Поволжье пациенты с ОП лечились ГП АЛН достоверно реже, чем больные в других регионах стран (p=0,007). Пациенты, диагноз ОП которым поставили гинекологи и неврологи, принимали только ГП АЛН, в то время как больные, наблюдавшиеся у ревматологов, терапевтов, эндокринологов и травматологов, использовали их достоверно реже (p=0,048). Бесплатно больные ОП обеспечивались только ГП АЛН, оригинальный препарат приобретался пациентами самостоятельно за свой счет.
Больные, принимавшие в течение последнего года ГП, заменяли лекарственные средства для лечения ОП почти в 2 раза чаще (13,6%), чем использовавшие оригинальный АЛД (7,4%; p=0,19), но и те, и другие пропускали прием антиостеопоротических средств в одинаковом проценте случаев (29 и 24% соответственно; p=0,41).
Среди лиц, принимавших оригинальный АЛН, комплаентными в течение года были 57% больных, среди получавших ГП – 44,5% (p=0,064). Приверженность была выше у пациентов с продолжительностью болезни 1 год: 78 и 54% для оригинального и генерического препаратов соответственно (p=0,046). У больных с длительностью ОП 3 года и более приверженность лечению составила 27 и 35% соответственно (p=0,6).
К причинам замены лекарственного препарата у лечившихся АЛН отнесены стоимость препарата, которую отметили 60% больных, отсутствие рекомендованного препарата в аптеке (23%), совет врача или работника аптеки (6%), плохая переносимость ранее принимаемого средства (5%), отсутствие эффекта от проводимого лечения (2%).
Пациентов также просили указать причины пропуска в приеме препарата. Для ГП АЛН это были стоимость лекарства (57%), длительность лечения (42%), отсутствие препарата в аптеке (24%), неудобство приема (15%), плохая переносимость (14%) или они просто забывали о дне очередного приема (4%). Среди принимавших оригинальный АЛН 73% пропускавших прием больных указали на высокую стоимость лечения, 45% – на длительность терапии и 27% – на отсутствие препарата в аптеке.
Таким образом, проведенные нами опросы показали, что в реальной клинической практике ГП АЛН нашли широкое применение: врачи их рекомендовали чаще, чем другие антирезорбтивные средства для лечения ОП, и 62% больных ОП предпочитали их в качестве основной терапии в течение года, предшествовавшего анкетированию. По данным агентства IMS Health (http://www. imshealth.com), в 2015 г. на долю всех ГП (помимо АЛН учитывались генерики ризедроната и золедроновой кислоты, а также этидроновой кислоты) приходилось 50,3% от числа всех проданных упаковок лекарственных средств для лечения ОП, что в целом согласуется с результатами наших опросов.
Можно предположить, что мотивацией врачей к назначению ГП была уверенность 81% из них в том, что из-за стоимости лечения пациенты могут не начать терапию ОП или прекратить ее досрочно, а для достижения значимого результата в профилактике переломов требуется длительное применение антиостеопоротических препаратов. Около 60% врачей в Греции и на Кипре также считали, что собственные расходы пациента на лечение служили для них главным фактором для рекомендации ГП [5].
Для пациентов с ОП материальные затраты на лечение были одной из детерминант, влиявших на выбор лекарственного средства и длительность его использования. Более половины опрошенных нами больных заменяла препараты или пропускала их прием из-за высокой, по их мнению, стоимости рекомендованного лекарства. Наверное, не случайно среди принимавших ГП АЛН было больше лиц, указавших на замену терапии: они перешли на них с приема оригинального препарата, т.к. лечиться ими было дешевле. Во многих странах экономический фактор также влияет на приверженность пациентов терапии. Было показано, что 55,5% случаев непродления больным рецепта врачом были связаны со стоимостью препарата или отсутствием страхового покрытия [6], а пациенты с более высокими фактическими расходами на лечение в 13–39% случаев были менее склонны к его продолжению [7]. Среди больных ОП в США оригинальным АЛН преимущественно лечились лица с высоким доходом или имевшие право на получение дополнительных субсидий на лекарственное обеспечение [8].
В нашем исследовании комплаентность больных, лечившихся как ГП, так и оригинальным АЛН, составила в среднем 47%, что согласуется с результатами работ зарубежных и отечественных авторов [9, 10]. Но оказалось, что пациенты с меньшей длительностью заболевания были более привержены приему оригинального препарата, в то время как лица, имевшие более длительный стаж болезни, чаще использовали ГП. Аналогичные данные были получены в Италии, где в реальной клинической практике среди 20 711 пациентов с ОП в возрасте старше 73 лет, начавших терапию генерическим или оригинальным АЛН, после 34 месяцев наблюдения не было выявлено статической разницы в комплаентности между группами лиц, принимавших эти лекарства, а данные по продолжительности лечения были в пользу ГП [11]. В то же время van J.F. Boven и соавт. не обнаружили разницы в однолетней приверженности больных лечению ГП или оригинальным АЛД (отношение шансов [ОШ] – 1,00; 95% доверительный интервал [ДИ] – 0,89–1,12) [12].
Однако, по данным канадской базы Régie de l’Assurance Maladie du Québec, пациенты, начавшие лечиться ГП АЛН, в течение первого года терапии имели более высокий риск досрочного прекращения лечения (ОШ – 2,08; 95% ДИ – 1,89–2,28), чем принимавшие оригинальный препарат (p<0,001) [13]. В Швеции перевод больных ОП с оригинального АЛН на его ГП был ассоциирован со снижением их приверженности лечению (ОШ – 1,25; 95% ДИ – 1,2–1,3): число пациентов, принимавших генерики АЛН, увеличилось с 11 до 45%, в то время как общее число лиц, продолжавших терапию в течение года, уменьшилось с 67 до 52% [14]. В США переход 81% пациентов из 15 310 человек, ранее получавших оригинальный АЛН, на ГП сопровождался незначительным повышением числа лиц, досрочно прекративших лечение: с 7,7 до 8,9% (ОШ – 1,15; 95% ДИ – 1,05–1,26). Авторы сделали следующий вывод: внедрение в практику ГП существенно не повлияло на приверженность пациентов лечению ОП [8].
Многие исследователи отмечают, что нежелательные явления, связанные с приемом лекарственных средств, служат основной причиной низкой приверженности лечению и влияют на длительность их приема пациентами с ОП [15, 16]. В крупном исследовании розничной аптечной сети США было установлено, что нежелательные явления на фоне приема БФ послужили причиной их отмены в 67% случаев [17]. По мнению 22% опрошенных нами врачей, нежелательные явления могут быть причиной отказа пациента от продолжения лечения на фоне терапии любыми антиостеопоротическими препаратами. В свою очередь опрошенные нами пациенты, пропускавшие прием ГП АЛН, в 14% случаев ссылались на плохую переносимость лечения, а среди принимавших оригинальный препарат таких лиц не было. При этом нельзя не отметить, что 5% больных, принимавших на момент опроса ГП АЛН, на предшествовавшей терапии по поводу ОП уже имели нежелательные явления, которые привели к замене лекарственного средства. В проспективном наблюдательном исследовании MUSIC-OS, проходившем в 5 странах Европы и Канаде, 69,1% женщин старше 55 лет с ОП сообщили о наличии у них симптомов поражения желудочно-кишечного тракта (ЖКТ) на фоне антиостеопоротической терапии, что было достоверно больше, чем среди лиц с впервые установленным диагнозом ОП, которые данного лечения не получали (p<0,03). В дальнейшем у пациентов с поражением ЖКТ в анамнезе отмечали более низкие комплаентность и удовлетворенность лечением, чем у больных без нарушений со стороны ЖКТ[18].
Прекращение приема пероральных БФ в большинстве случаев связано с их негативным влиянием на ЖКТ [19, 20]. При этом высказываются предположения, будто плохая переносимость ГП АЛН обусловлена их более быстрой дезинтеграцией, которая может повышать вероятность локального раздражения слизистой оболочки пищевода под воздействием прилипших кристаллов лекарственного вещества («таблеточный эзофагит») [19, 21]. На возникновение эзофагита во время терапии таблетированными БФ помимо действия непосредственно активной субстанции оказывают влияние такие факторы, как возрастное ухудшение перистальтики пищевода, локальная кислотность, количество воды, которой запивается лекарство, положение пациента после приема препарата, размер, форма и оболочка лекарственного средства [22]. Сам АЛН в водном растворе имеет низкий уровень pH и поэтому может выступать в качестве раздражителя слизистой оболочки пищевода и желудка. При наличии у больного кислотного гастроэзофагеального рефлюкса местное повреждающее действие АЛН усиливается, а ослабление кислотного воздействия на слизистую ЖКТ служит основным способом лечения при эзофагите, обусловленном приемом АЛН [23].
С целью снижения до минимума контакта частиц АЛН со слизистой оболочкой верхних отделов ЖКТ и предотвращения увеличения кислотности желудочного сока, что уменьшает вероятность повреждения слизистой пищевода в случае рефлюкса из желудка, был разработан новый ГП Биносто (SwissKo, Швейцария) в виде шипучих таблеток АЛН, которые полностью растворяются в воде с образованием буферного раствора.
Биодоступность Биносто сопоставима с таковой обычно принимаемой таблетки оригинального АЛН, которая при приеме натощак утром за 2 часа до стандартного завтрака составляла 0,64% у женщин и 0,60% у мужчин, а за час или полчаса до еды – 0,46 и 0,39% соответственно. Однако для шипучих таблеток внутрииндивидуальные различия в экскреции (и следовательно, во всасывании) были меньшими: коэффициент вариации общей экскреции в течение первых 48 часов – 32,0 против 42,1%, коэффициент вариации максимальной скорости экскреции – 37,5 против 45,6% [20].
Исследования по биоэквивалентности проведены во многих странах, где была зарегистрирована данная форма АЛН. В России было проведено проспективное открытое рандомизированное перекрестное сравнительное фармакокинетическое исследование шипучей лекарственной формы АЛН (Биносто 70 мг) и оригинального АЛН 70 мг, в котором приняли участие 42 здоровых добровольца (мужчины и женщины) в возрасте от 18 до 43 лет. Доверительные интервалы для средних значений параметров биоэквивалентности при приеме тестируемого и оригинального препаратов находились в пределах 93–106%, что позволило зарегистрировать шипучие таблетки Биносто 70 мг для лечения ОП у женщин в постменопаузе и у мужчин.
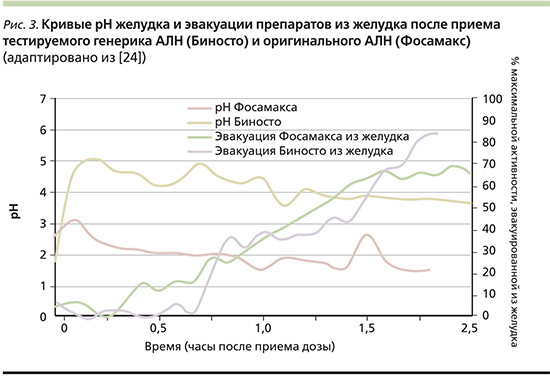
Проведенное одноцентровое открытое рандомизированное перекрестное исследование по оценке опорожнения содержимого желудка после приема меченых 99mTc-ДТПА таблеток оригинального АЛН или новой шипучей лекарственной формы ГП, обладающей высокой буферной способностью, посредством сцинтиграфии и определения рН желудка с использованием назогастральных зондов показало, что шипучая лекарственная форма АЛН полностью поступила в желудок без удерживания в пищеводе, а время нахождения в желудке буферного раствора достоверно не увеличивалось по сравнению с таковым при приеме брендового препарата [24]. Это свидетельствует о том, что при приеме буферного раствора Биносто не надо увеличивать время нахождения пациента утром натощак для лучшей абсорбции препарата в ЖКТ. Кроме того, было установлено, что после введения растворенного генерика АЛН значение рН желудка сразу доводилось до более высоких уровней (рН>3), что способствовало снижению кислотности желудочного сока. В группе лиц, получавших таблетированный оригинальный АЛН, была выявлена более высокая кислотность (рис. 3), что оказалось негативным фактором для слизистой оболочки верхних отделов ЖКТ.
Генерик АЛН Биносто применяется для лечения ОП с 2012 г., в настоящее время он лицензирован более чем в 60 странах. Преимуществом нового препарата является и то, что его растворяют в 120 мл воды, в то время как таблетку АЛН надо запивать целым ее стаканом (200 мл) для лучшего прохождения по пищеводу. За 4 года применения в постмаркетинговых базах данных зарегистрировано лишь 23 нежелательных явления, связанных с поражением ЖКТ, из них лишь один случай эрозивного эзофагита.
Таким образом, проведенное нами исследование по изучению применения различных антиостеопоротических препаратов больными ОП продемонстрировало широкое использование в клинической практике ГП АЛН. Доказанная эффективность оригинального АЛН и ценовая доступность воспроизведенных препаратов способствовали тому, что ГП назначались врачами чаще, чем другие антирезорбтивные средства, и больше половины больных использовали их в качестве основного средства терапии ОП. Однако приверженными лечению были лишь 47% пациентов, получавших АЛН. Одним из факторов, способствовавших отмене препарата,стала плохая его переносимость. Применение новой лекарственной формы АЛН (Биносто 70 мг) в виде шипучих таблеток, употребляемых в виде буферного раствора с клубничным вкусом, уменьшающих кислотность желудочного сока, что приводит к снижению его негативного действия на слизистую оболочку верхних отделов ЖКТ, может способствовать повышению приверженности пациентов лечению ОП.



