Введение
Как известно, тиазидные и тиазидоподобные диуретики являются краеугольным камнем в лечении артериальной гипертензии (АГ), обеспечивают эффективную начальную антигипертензивную монотерапию и служат основой многокомпонентной антигипертензивной стратегии [1–3]. Исследование антигипертензивного, кардио- и вазопротективных эффектов тиазидоподобного диуретика индапамида, в т.ч. в нейтральных дозах в метаболическом отношении, выявило широкий спектр фармакодинамических механизмов терапевтического действия при АГ [3, 4].
Сосуды сопротивления являются плацдармом для реализации различных патогенетических механизмов АГ, а также одними из главных детерминант прогрессирования заболевания и поражения органов-мишеней [2, 5]. В связи с этим современная стратегия адекватной антигипертензивной терапии предполагает также достижение регрессии ремоделирования сосудов и коррекцию дисфункции эндотелия [2, 6].
По результатам многоцентровых рандомизированных клинических исследований доказаны безопасность и стабильный антигипертензивный эффект ретардной формы индапамида в дозе 1,5 мг/сут, адаптированной к лечению АГ, в т.ч. в виде стартовой терапии [1, 2, 7–9]. Однако до сих пор дискутируется вопрос о влиянии тиазидных диуретиков на вегетативный контроль сердечно-сосудистой системы и нередко допускается потенциально стимулирующее действие препаратов этого класса на симпатический отдел вегетативной нервной системы у пациентов с АГ [10]. В ранних публикациях, в т.ч. по результатам рандомизированных клинических исследований, установлена нейтральность или стимулирующее влияние тиазидных и тиазидоподобных диуретиков в отношении симпатоадреналовой системы [11]. Также подтверждено, что неблагоприятные метаболические эффекты, в т.ч. вследствие стимуляции симпатической нервной системы (СНС), при использовании данного класса антигипертензивных препаратов носят дозозависимый характер [5, 12]. Необходимо отметить, что при использовании тиазидоподобных диуретиков в дозах, не обладающих заметным натрийуретическим/диуретическим действием, реципрокной активации СНС не наблюдается [1, 2, 13].
Как известно, общепринятая концепция создания ретардных форм лекарств или с пролонгированным действием требует увеличения дозы активного вещества в 2–3 раза. Однако в препарате Индапамида ретард вместо 2,5 мг/сут индапамида с «немедленным высвобождением субстанции», рекомендованного первоначально в терапии АГ, предложено уменьшение дозы до 1,5/сут [3, 8]. Таким образом, несмотря на выявленные различные фармакодинамические механизмы, вазомоторные эффекты индапамида ретард у пациентов с АГ изучены недостаточно [3, 6, 7]. Также следует отметить, что связь вегетативной регуляции сердца с тяжестью эссенциальной АГ у пациентов, получающих длительную антигипертензивную терапию, недостаточно известна [13, 14]. Это представляет большой интерес для изучения антигипертензивной эффективности и влияния индапамида ретард на ремоделирование сердечно-сосудистой системы у пациентов с АГ в зависимости от исходного тонуса вегетативной нервной системы.
Целью исследования стала оценка эффективности Индапамида ретард в зависимости от наличия ремоделирования сосудов и вариабельности ритма сердца (ВРС) при неосложненном течении эссенциальной АГ.
Методы
В открытое клиническое исследование были включены 75 пациентов (43 мужчины и 32 женщины) с АГ I–II степеней, в возрасте от 48 до 60 лет (в среднем 56,3±6,4 года). Необходимо отметить, что пациенты, включенные в исследование, ранее не получали антигипертензивных препаратов постоянно, пользовались короткодействующими препаратами только для купирования эпизодов повышения артериального давления (АД), а также у отдельных пациентов имела место впервые выявленная АГ. Это позволило выполнять исходные инструментальные исследования непосредственно перед началом терапии изучаемым препаратом.
После скринингового обследования пациентов разделили на 2 группы: 1-я – 30 пациентов с нормальными структурно-функциональными показателями плечевой артерии (ПА) и 2-я группа – 45 пациентов с признаками ремоделирования сосудистой стенки и/или нарушенной вазомоторной функцией, т.е. толщина комплекса интима-медиа (КИМ) ПА более 0,9 мм и прирост величины эндотелий-зависимой вазодилатации (ЭЗВД) менее 10% после пробы с реактивной гиперемией [2]. В обеих группах пациентам назначали индапамид ретард 1,5 мг/сут («Канонфарма», Россия). Клиническая характеристика пациентов показала, что по гендерно-возрастному признаку, степени и давности АГ, а также по среднесуточным показателям систолического и диастолического АД (САД, ДАД) различия в сравниваемых группах недостоверны (табл. 1). Однако во 2-й группе по сравнению с 1-й показатель толщины КИМ ПА был достоверно выше (в среднем 29,3%; p<0,001), а величина ЭЗВД, наоборот, достоверно ниже.
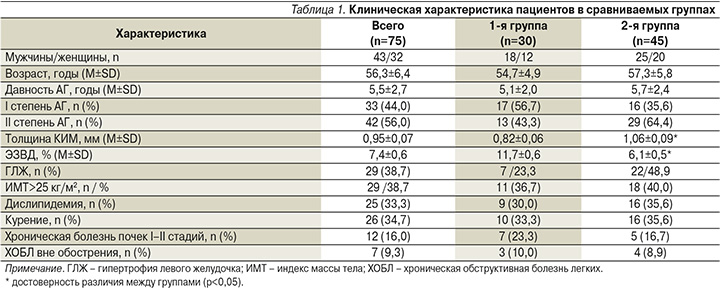
Кроме того, 29 (38,7%) пациентам диагностировали гипертрофию левого желудочка (ГЛЖ), в т.ч. в 1-й группе 7 (23,3%) пациентам, во 2-й – 22 (48,9%): χ2=1,78 (p=0,182). По данным суточного мониторирования АД (СМАД), у 32 (42,7%) пациентов выявлен суточный профиль АД типа диппер и у 43 (57,3%) – типа нон-диппер. При этом в 1-й группе по сравнению со 2-й преобладали случаи с типом диппер (66,7 против 26,7%), во 2-й, наоборот, пациентов с типом нон-диппер было в 2 раза больше, чем в 1-й (73,3 против 33,3%). Факторы риска, такие как курение, дислипидемия и избыточная масса тела, в группах различались недостоверно. Кроме того, хроническую болезнь почек I–II стадий диагностировали в 1-й группе у 23,3% пациентов, во 2-й – у 16,7%, а ХОБЛ в стадии вне обострения – у 10,0 и 8,9% пациентов соответственно. С учетом коморбидных состояний пациенты также получали корригирующее лечение, в частности статины в рекомендуемых дозах. Следует отметить, что частота применения, суточные дозы и спектр используемых липидснижающих препаратов в обеих группах существенно не различались.
Критерии невключения в исследование: симптоматические АГ, пациенты-«плацебо-реакторы», АГ «белого халата», ассоциированные клинические состояния при АГ, наличие сахарного диабета, хроническая сердечная недостаточность выше IIА-стадии и/или II функционального класса, постоянная форма фибрилляции предсердий и частая экстрасистолия.
Больным до и после 6 месяцев терапии Индапамидом ретард 1,5 мг/сут проводили инструментальные исследования. Исследование было выполнено в соответствии со стандартами надлежащей клинической практики (Good Clinical Practice) и принципами Хельсинкской декларации Всемирной медицинской ассоциации «Рекомендации для врачей, занимающихся биомедицинскими исследованиями с участием людей». Протокол исследования одобрен Этическим комитетом института. До включения в исследование все пациенты подписали письменное информированное согласие.
Допплер-эхокардиографическое исследование проводили на аппарате Acuson-X300 («Siemens-Acuson», Германия), оснащенном фазированным электронным датчиком в режимах В- и М-сканирования по стандартной методике. Вычисляли следующие показатели [2]: конечный систолический и конечный диастолический объемы левого желудочка (КСО ЛЖ, КДО ЛЖ), толщину межжелудочковой перегородки (МЖП) и задней стенки (ЗСЛЖ), фракцию выброса (ФВ), массу миокарда ЛЖ (ММЛЖ), сердечный индекс (СИ) и удельное периферическое сосудистое сопротивление (УПСС). ГЛЖ диагностировали при величине индекса ММЛЖ (ИММЛЖ) более 115 г/м2 у мужчин и более 95 г/м2 у женщин [1, 2].
С помощью ультразвукового допплеровского исследования ПА до и после реактивной гиперемии определяли диаметр просвета ПА, толщину КИМ, отношение толщины КИМ к диаметру просвета ПА (индекс С/П) и максимальную (систолическую) линейную скорость кровотока (Vmax). ЭЗВД изучали с помощью метода реактивной гиперемии, предложенного D.S. Celemajer et al. [2] и эндотелий-независимую вазодилатацию (ЭНЗВД) – по расширению сосуда после приема 0,5 мг нитроглицерина сублингвально.
Суточное мониторирование АД проводили согласно рекомендациям [2] на аппарате BPLab (Россия). Регистрация АД выполнялась с интервалом 30 минут днем и 1 час ночью. Периоды бодрствования и сна выставляли индивидуально в реальном времени и полученные данные анализировали с учетом дневников самонаблюдения. Вычисляли среднесуточные показатели САД и ДАД (cр. САД, cр. ДАД), частоту сердечных сокращений (ЧСС), степень ночного снижения (СНС) САД и ДАД, вариабельность САД и ДАД (вар. САД, вар. ДАД), индексы времени «нагрузки давлением» (ИВ САД, ИВ ДАД), величину утреннего подъема (ВУП) САД и ДАД, соотношение остаточного гипотензивного эффекта к максимальному эффекту (индекс t/p, %). С учетом величины суточного индекса САД и ДАД определяли типы суточного профиля АД.
ВРС изучали при холтеровском мониторировании ЭКГ с помощью аппарата «Astracard» (Россия) [15]. Анализ показателей ВРС производили в 5-минутных отрезках при 24-часовой записи электрокардиограммы (ЭКГ). Определяли следующие временные показатели ВРС: 1) средняя продолжительность синусовых интервалов R-R (NN); 2) стандартное отклонение от средней длительности всех синусовых интервалов R-R (SDNN); 3) средняя для стандартных отклонений от средних значений интервалов NN на всех 5-минутных участках записи ЭКГ (SDNN index); 4) среднеквадратичное различие между продолжительностью соседних синусовых интервалов R-R (RMSSD); 5) процент от общего числа последовательных пар интервалов R-R, различающихся более чем на 50 мс (pNN50). Также определяли спектральные (частотные) показатели ВРС: высокочастотный компонент мощности (HF), низкочастотный компонент (LF), очень низкочастотный компонент (VLF), соотношение LF/HF. Также вычисляли нормализованные единицы частотных компонентов HF и LF (HFn, LFn.) для нивелирования влияния на них общей мощности.
Статистический анализ проводили с помощью программы Statistica 8.0 для Windows. Нормальность распределения переменных определяли согласно тесту Колмогорова–Смирнова. Для определения центральной тенденции и разброса непрерывных переменных при распределении, близком к нормальному, вычисляли среднюю арифметическую (M) и стандартное отклонение (SD). Достоверность различия переменных в двух группах определяли с помощью параметрических или непараметрических методов в зависимости от нормальности распределения переменных. Для сравнения долей применяли точный критерий Фишера и χ2-критерий Пирсона.
С целью изучения корреляции использовали метод ранговой корреляции Спирмена. Различия считали статистически значимыми при р<0,05.
Результаты
На фоне терапии целевые уровни АД в 1-й группе были достигнуты 16 (53,3%) пациентами, во 2-й группе – 29 (64,4%), при этом у всех пациентов обеих групп наблюдалась нормализация АД (ниже 140/90 мм рт.ст.). Среднесуточные показатели САД и ДАД в группах снизились достоверно, однако различие между группами было недостоверным (табл. 2).

Динамика показателей ИВ САД и ИВ ДАД в обеих группах оказалась сопоставимой и свидетельствует о стабильном и надежном контроле АД в течение суток. На фоне терапии также отмечено достоверное снижение показателей ВУП САД и ВУП ДАД, более выраженное в 1-й группе. Это подтверждается и показателями индекса t/p выше 50%, которые свидетельствуют о достаточно выраженном пролонгированном антигипертензивном эффекте Индапамида ретард в течение суток.
При оценке структурно-функциональных показателей сердца и сосудистой стенки через 6 месяцев терапии Индапамидом ретард выявлены некоторые различия в группах (табл. 3).

Так, уменьшение величин ИММЛЖ у пациентов с ГЛЖ в основном за счет толщины стенок ЛЖ в 1-й группе составило в среднем 10,2% (p=0,021), во 2-й – 13,6% (p=0,007). Показатели насосной функции сердца – СИ и ФВ, на фоне терапии в группах изменились незначительно и неоднозначно (p>0,05). Однако достоверное снижение показателя УПСС выявлено во 2-й группе и в среднем составило 17,1% (p=0,002). Кроме того, только во 2-й группе отмечена достоверная динамика показателей трансмитрального диастолического потока (Ve, Va, Ve/Va, ВИВР), свидетельствующая об улучшении релаксации миокарда ЛЖ, что, вероятно, связано с регрессией ГЛЖ на фоне терапии Индапамидом ретард. На фоне терапии Индапамидом ретард во 2-й группе произошли значительные сдвиги структурно-функциональных показателей ПА, в частности достоверно уменьшилась толщина КИМ в среднем на 12,8% (p=0,013) и, наоборот, увеличилась величина ЭЗВД в среднем на 25,4% (p<0,001). В результате во 2-й группе отмечено выраженное снижение постнагрузки – показателя УПСС в среднем на 17,1% (p<0,001).
Сравнение исходных показателей ВРС в группах показало, что в 1-й группе как временные, так и частотные параметры ВРС свидетельствуют о преобладании тонуса СНС, во 2-й наблюдается снижение тонуса как СНС, так и парасимпатической нервной системы по сравнению с 1-й группой (табл. 4).

Также выявлено, что число пациентов с критическими значениями показателей SDNN <50 мс и LF/HF>1,5, имеющих неблагоприятное прогностическое значение, которые подтверждают повышенную активность СНС, в 1-й группе было достоверно выше, чем во 2-й: 56,7 против 31,1% (χ2=4,85; p=0,027) и 63,3 против 26,7% (χ2=9,98; p=0,002) соответственно. Необходимо отметить, что через 6 месяцев после терапии Индапамидом ретард изменения показателей ВРС в группах оказались недостоверными (p>0,05), а также сохранялись межгрупповые различия показателей, что свидетельствует об отсутствии модуляции нейрогуморальной регуляции сердечно-сосудистой системы.
Также выявлена прямая корреляция между показателями SDNN и ЭЗВД (рисунок). При этом, несмотря на незначительные изменения показателя SDNN, величина ЭЗВД после терапии Индапамидом ретард увеличивается существенно, что подтверждает роль прямого сосудистого действия препарата вне зависимости от вагосимпатического баланса у пациентов с АГ.

Обсуждение
В контролируемых клинических исследованиях Индапамид SR в дозе 1,5 мг/сут снижал как среднее САД, так и ДАД у пациентов с эссенциальной гипертензией или изолированной систолической гипертензией [8, 9]. Снижение САД и ДАД при применении Индапамида SR было таким же, как при применении амлодипина 5 мг/сут, кандесартана 8 мг/сут и эналаприла 20 мг/сут [3]. Полученные нами результаты исследования также показали достаточно высокое антигипертензивное действие Индапамида ретарда в дозе 1,5 мг/сут у пациентов с неосложненной АГ I–II степеней. Также выявлена автокорреляция степени регрессии ремоделирования сосудистой стенки с исходными показателями, характеризующими выраженность эндотелиальной дисфункции и утолщения КИМ. Это подтверждается динамикой структурно-функционального ремоделирования сосудистой стенки на фоне терапии Индапамидом ретард во 2-й группе. Таким образом, показано, что Индапамид ретард обладает таргетированным сосудистым действием на пациентов с АГ даже при наличии ранних субклинических признаков ремоделирования сосудов – гипертрофии медиа и/или эндотелиальной дисфункции.
Указанное вазопротективное действие препарата, вероятно, обусловлено способностью стимулировать эндогенный синтез оксида азота эндотелием артерий [4, 6], а также снижением реактивности артериол на вазоконстрикторные агенты, в т.ч. на катехоламины, вследствие снижения содержания ионов натрия в их стенке [7, 8]. Этому также способствует слабовыраженный натрийуретический эффект Индапамида ретард по сравнению с обычным индапамидом в дозе 2,5 мг. Согласно клиническим рекомендациям, тиазидные и тиазидоподобные диуретики рекомендуются пациентам с изолированной систолической АГ, обусловленной повышенной ригидностью крупных артерий как препараты первой линии терапии [1, 2].
Противоречивые данные получены в отношении корреляции вегетативной дисфункции с ремоделированием кардиоваскулярной системы и антигипертензивным действием Индапамида ретард при АГ [13, 14]. Так, установлено, что на ранних стадиях эссенциальной АГ, как правило, преобладает симпатическая активность и это позволяет предположить, что нейрогормональная дисрегуляция может быть ключом к ее этиологии и прогрессированию, а также для выбора антигипертензивной терапии [10]. H. Mussalo et al. [11] по результатам сравнительной оценки ВРС у здоровых субъектов и у пациентов с легкой и тяжелой степенями эссенциальной АГ показали, что преобладание тонуса СНС прямо коррелирует с тяжестью АГ. Также подчеркивается, что у пациентов с тяжелой степенью АГ четкой ассоциации между показателем SDNN и уровнем АД не выявлено [3]. Как известно, длительное применение различных классов антигипертензивных препаратов может изменить корреляции показателей ВРС и уровней АД [7]. Так, выявлено, что корреляции показателей ВРС и уровней АД статистически более значимы для группы пациентов, не принимавших антигипертензивных препаратов [14].
Также следует отметить, что роль вегетативной дисфункции в ремоделировании сосудов пациентов разных категорий с АГ изучена недостаточно. Было показано, что в начальной неосложненной стадии АГ, т.е. в отсутствие ремоделирования сосудов и/или эндотелиальной дисфункции симпатическая гиперактивность выражена значительнее, чем у пациентов со структурно-функциональным ремоделированием артерий мышечного типа и ГЛЖ. Это, возможно, объясняется тем, что на поздних стадиях АГ происходит истощение запасов нейромедиаторов СНС и нередко наблюдается параллельное снижение вагусной и симпатической активности [10].
Изучение роли вегетативной дисфункции при различных стадиях эссенциальной АГ важно для выбора эффективных терапевтических стратегий антигипертензивной терапии [13]. Так, полученные нами результаты свидетельствуют об обратимости гипертрофии сосудистой стенки и улучшении эндотелиальной функции в группе пациентов, имевших признаки гипертензивного ремоделирования сосудов, на фоне терапии Индапамидом ретард. Выявленная прямая корреляция показателей SDNN и ЭЗВД свидетельствует: увеличение вазодилатации на фоне терапии Индапамидом ретард ассоциируется со сниженной симпатической активностью. Важно отметить, что при терапии Индапамидом ретард 1,5 мг/сут усиления симпатической активности вне зависимости от исходных нарушений вагосимпатического баланса нами не выявлено.
Необходимо отметить, что установлены различные фармакологические механизмы, подтверждающие первично сосудистые эффекты индапамида [3, 4, 8]. Так, индапамид вызывает усиление синтеза простагландина Е2 и простациклина, которые активируют депрессорное звено регуляции сосудистого тонуса [4]. Установлено, что вазодилатирующее действие индапамида связано с уменьшением внутриклеточной концентрации ионообменного кальция в гладкомышечных клетках артериол, напоминающий эффект блокады медленных кальциевых каналов, характерной для дигидропиридиновых блокаторов кальциевых каналов [6, 9]. Кроме того, подтверждена роль индапамида в стимуляции эндотелием синтеза оксида азота [3, 12]. Предполагается, что одним из возможных механизмов вазодилатирующего действия является агонизм индапамида в отношении калиевых каналов мембран гладкомышечных клеток [5]. Поэтому, исходя из фармакотерапевтических эффектов, индапамид расценивается специалистами как периферический вазодилататор. Все это позволяет рекомендовать широкое применение индапамида с «пролонгированным высвобождением субстанции» в качестве моно- и комбинированной терапии всех категорий гипертоников.
Заключение
Таким образом, можно констатировать, что антигипертензивный, кардио- и вазопротективные эффекты Индапамида ретард реализуются за счет различных фармакологических механизмов в зависимости от нарушений вагосимпатического баланса и ремоделирования сосудов сопротивления. Показано, что в отсутствие структурно-функциональных изменений сосудов основным патогенетическим механизмом АГ является нарушение нейрогуморальной регуляции кровообращения, что характерно для начальных стадий заболевания. По мере прогрессирования АГ ремоделирование резистивных сосудов становится ведущим патогенетическим механизмом АГ при нормальной или даже сниженной симпатической активности. Широкий терапевтический диапазон индапамида позволяет рассматривать его как универсальный антигипертензивный препарат для адекватной коррекции АГ. С учетом актуальности оценки нарушений вегетативной регуляции у пациентов, получающих длительно антигипертензивную медикаментозную терапию, необходимо проведение контролируемых клинических исследований для установления эффективности тиазидоподобного диуретика в виде монотерапии или комбинации с альтернативными антигипертензивными препаратами с учетом особенностей клинического течения и поражений сердечно-сосудистой системы.
Вклад авторов. Б.Г. Искендеров – концепция и дизайн исследования, написание текста и редактирование. Т.В. Лохина – сбор и обработка материала. Н.В. Беренштейн – статистическая обработка данных.



