Введение
Синдром Ашермана (СА) – это патологическое состояние, при котором в полости матки образуются соединительно-тканные сращения (внутриматочные синехии), что сопровождается деформацией полости матки и функциональными нарушениями [1]. Впервые эту патологию упомянул в 1894 г. немецкий акушер-гинеколог Генрих Фритч (Heinrich Fritsc; 1844–1915, Германия) [2]. Затем заболевание было подробно описано в 1948 г. Джозефом Ашерманом (Joseph Asherman; 1889–1968; Чехия–Израиль), который обнаружил, что после повторных выскабливаний стенок полости матки у женщин исчезают менструации и развивается рубцовая ткань (синехии) в области внутреннего зева шейки и/или между внутренними стенками матки [3].
В настоящее время СА не теряет своей актуальности, т.к. сопровождается высокой частотой бесплодия, привычного невынашивания, осложнений беременности, аменореи и гипоменструального синдрома. Патологические изменения в матке наблюдаются в 54% случаев женского бесплодия, в 41% – при нарушениях функции эндометрия [4]. СА встречается при эндометриозе различной степени тяжести, а также может быть причиной привычного невынашивания беременности [5]. А. Baradwan et al. обнаружили, что распространенность СА составляет 4,6% у бесплодных женщин [6]. В мета-анализе A.B. Hooker et al. СА установлен у 19,1% пациенток с выкидышем в анамнезе (в течение года после потери беременности) [7].
Одна из основных причин развития СА – механическая травма эндометрия [8], что возможно во время проведения различных внутриматочных манипуляций: лечебно-диагностическом выскабливании полости матки, хирургическом прерывании беременности, оперативном лечении, использовании внутриматочных контрацептивов, внутриматочных вмешательствах в раннем и позднем послеродовом периодах.
Предположить наличие СА можно на основании жалоб и анамнеза: отсутствие менструации или скудная менструация, предшествующие внутриматочные вмешательства, нарушение менструального цикла, отсутствие беременности (бесплодие I, II), болевой синдром, хронический эндометрит в анамнезе, осложнения в послеродовом периоде (остатки плацентарной ткани, ручное отделение последа, маточное кровотечение) [9].
Ультразвуковая картина СА неспецифична, характеризуется наличием нечетких и неровных контуров эндометрия, прерывистым контуром М-эхо, гипоплазией эндометрия, гипер- и гипоэхогенными тяжами. Сообщается, что трансвагинальное ультразвуковое исследование имеет очень ограниченные диагностические возможности с чувствительностью 52% и специфичностью 11% относительно гистероскопии [10]. Более информативна гидросонография, благодаря которой синехии визуализируются более четко в виде гипер-эхогенных перегородок, разделяющих полость матки на камеры с анэхогенным содержимым [11]. Контрастная соногистерография имеет высокую отрицательную прогностическую ценность (98%), но умеренную положительную прогностическую ценность (43%) по сравнению с гистероскопией. При проведении гистеросальпингографии выявляются дефекты наполнения разных форм и размеров [12]. «Золотым» стандартом диагностики внутриматочных синехий является гистероскопия. Во время исследования спайки определяются как белесоватые тяжи разной плотности и длины, а также как грубые сращения, которые соединяют стенки матки между собой [13]. Лечение СА сводится к восстановлению менструальной и репродуктивной функций, что достигается путем рассечения синехий во время гистероскопии тубусом гистероскопа, гистерорезектоскопом, эндоскопическими ножницами и щипцами, диодным лазером, монополярным электродом или биполярным зондом [9–10]. Использование лазера имеет ряд преимуществ: более мягкое воздействие на ткани, снижение риска возникновения ожогов, отсутствие электрохирургических осложнений, качественный гемостаз, возможность удаления патологических образований в труднодоступных местах (дно матки, маточные углы, перешеек, цервикальный канал), возможность выполнения процедуры через манипуляционный канал офисного гистероскопа, в т.ч. в амбулаторных условиях, а также низкая стоимость процедуры.
Актуальная на сегодня проблема лечения СА заключается в высоком риске рецидива, средняя частота которого после оперативного лечения внутриматочных синехий составляет 23–63% [10]. Для профилактики развития рецидивов используются гормональная терапия эстрогенами и гестагенами в циклическом режиме, при необходимости (инфекционном факторе) – антибактериальная терапия, противоспаечные барьеры на основе гиалуроновой кислоты, физиотерапия, гидролизаты плаценты человека, стволовые клетки [14–16].
Однако вопрос по-прежнему находится в стадии изучения и поиска оптимальных терапевтических воздействий, которые снизили бы риск рецидивов и повысили число успешных беременностей.
Цель исследования: оценить эффективность лечения пациенток с СА при использовании гистероскопического адгезиолизиса в комплексе с орошением полости матки кавитированными растворами, пелоидо- и магнитотерапией.
Методы исследования
Дизайн: проспективное открытое несравнительное клиническое исследование.
Оно проведено в 2015–2020 гг. на базе Центра оперативной гинекологии «Женская клиника», Екатеринбург, в соответствии с Хельсинкской декларацией ВМА (2008, Сеул), правилами Надлежащей клинической практики и другими применимыми в Российской Федерации нормативными документами. Все пациентки подписали информированное добровольное согласие на участие в исследовании.
В исследование включены 29 пациенток со спаечным процессом в полости матки (синдром Ашермана; N85.6 – внутриматочные синехии) различной степени тяжести, подтвержденным при диагностической гистероскопии.
Критерии включения: возраст – 18—45 лет, наличие внутриматочных синехий, подтвержденных диагностической гистероскопией, наличие информированного согласия на участие в исследовании.
Критерии исключения: возраст моложе 18 лет, период грудного вскармливания, острая стадия хронических заболеваний, злокачественные процессы любой локализации.
Методы обследования: сбор жалоб и анамнестических данных, общеклинические методы, принятые в акушерстве и гинекологии, общие лабораторные методы (госпитальный комплекс), функциональные методы: трансабдоминальное и трансвагинальное ультразвуковое исследование органов малого таза с оценкой толщины М-эхо и состояния эндометрия (аппарат Voluson Е8 Expert, датчики: объемный конвексный RAB-6P, внутриполостной RIC6-12-D), гистероскопия (К. Storz, оптика 30 гр., D4 мм). Оценка степени выраженности внутриматочных синехий проведена во время лечебно-диагностической гистероскопии, согласно классификации Европейской ассоциации гинекологов-эндоскопистов (1995).
В лечении пациенток применялась хирургическая гистероскопия, которая сопровождалась различными вариантами рассечения внутриматочных синехий: диодным лазером Лахта-Милон (ООО «Милон-Лазер», Санкт-Петербург, длина волны – 970 нм, мощность – 30 Вт), монополярным электродом, ножницами, биполярным зондом, тубусом гистероскопа, комбинированным методом (монополяр–ножницы, гистероскоп–ножницы). В большинстве случаев выполняли введение противоспаечного барьера в полость матки (5 мл геля антиадгезина, содержащего высокоочищенную натриевую соль гиалуроновой кислоты и карбоксиметилцеллюлозу натрия) сразу после завершения процедуры.
После оперативного вмешательства проводили комплекс лечебно-реабилитационных мероприятий, включивших циклическую гормональную терапию (препарат эстрадиол/дидрогестерон 2/10 мг в циклическом режиме по схеме 21/7 с 5-го дня после операции) в течение 3–4 месяцев, со 2-го месяца после операции выполняли орошение полости матки 0,05%-ным раствором водного хлоргексидина или раствором имунофана (50 мкг в разведении 1:100 в физиологическом растворе) кавитированным низкочастотным ультразвуком (НЧУЗ) продолжительностью 3–5 минут, на курс по 5 процедур ежедневно, всего – 2 курса. Для проведения орошения использовали ультразвуковой кавитационный аппарат АК101 (ООО «ФОТЕК», Екатеринбург). После завершения курса НЧУЗ с 5-го дня менструального цикла проводили пелоидотерапию с использованием геля на основе грязи Мертвого моря (ООО БиЛайфМед, Россия) в объеме 60 мл интравагинально, экпозицию 20 минут в сочетании с магнитотерапией на низ живота (Полюс-2Д, параметры: магнитная индукция – 40 мТл, длительность импульса – 12 мс, частота следования импульсов – 12,5 Гц) по 10 процедур, 1–2 курса.
После курса терапевтических мероприятий (в цикле, следующем после его окончания) выполнялось контрольное УЗИ. Проводили динамическую диагностическую офисную гистероскопию через 3–4 месяца после оперативного вмешательства, при обнаружении рецидива – повторное рассечение спаек.
Период наблюдения за пациентками в послеоперационном периоде составил от 1,5 до 6 лет.
Критерии оценки результатов лечения: первичные – восстановление менструального цикла, отсутствие данных за наличие синехий в полости матки по данным УЗИ и диагностической гистероскопии через 3–4 месяца; вторичные – наступление беременности в течение 12 месяцев после операции.
Статистический анализ полученных данных осуществляли при помощи пакета программ «Statistica for Windows 10.0» (StatSoft® Inc., США). Применяли методы описательной статистики. Количественные показатели представляли в виде М (SD), где М – среднее значение, SD – среднее квадратичное отклонение. Закон распределения признаков оценивали при помощи критерия Колмогорова–Смирнова. Для показателей, характеризующих качественные признаки, указывали абсолютное число и относительную величину в процентах (В.М. Боровиков, 2001).
Результаты исследования
Средний возраст пациенток составил 40,3 (±6,9) года. Общая клиническая характеристика обследованных представлена в таблице.
При обращении пациентки предъявляли жалобы: на аменорею – 6 (20,6%), олиго- и опсоменорею – 9 (31%), постменструальное кровомазанье – 6 (20,6%), дисменорею – 9 (31%), не предъявляли жалоб – 3 (10,3%).
При гистероскопии I степень СА диагностирована у 4 (13,7%) пациенток, II – у 9 (31%), III – у 9 (31%), IV – у 4 (13,7%), V – у 2 (6,8%). Синехии цервикального канала определились у 10 (34,5%) пациенток, у одной обнаружена полная облитерация цервикального канала.
Во время гистероскопии проведено рассечение синехий диодным лазером «Лахта Милон» 14 (48,3%) пациенткам, монополярным электродом – 3 (10,3%), ножницами – 2 (6,8%), биполярным зондом – 3 (10,3%), гистероскопом – 7 (24%), комбинированная хирургия (монополяр–ножницы, гистероскоп–ножницы) – 5 (17,2%). Введение 5 мл антиадгезина в полость матки сразу после вмешательства выполнено 16 (55%) пациенткам.
Первичные результаты лечения. Восстановление менструальной функции произошло у 20 (76,9%) пациенток в течение 3–6 месяцев (при исходной частоте нарушений менструального цикла у 26 пациенток). Толщина М-эхо, по данным УЗИ, до лечения была 6,5 (±0,11) мм, после лечения – 6,2 (±0,07) мм. Отсутствие синехий отмечено у 23 (79,3%) пациенток в течение 3–4 месяцев после операции. Рецидив синехий выявлен у 6 (20,7%) пациенток за тот же период наблюдения, сращения были незначительными и разделены при контрольной гистероскопии методом оптической диссекции.
Вторичные результаты лечения. Из 19 пациенток, планировавших беременность, забеременели 10 (52,6%): у 8 наступила спонтанная беременность, у 2 – в результате ЭКО. У 7 (70%) из них беременность завершилась родами: кесарево сечение – у 4 (57,1%), роды через естественные родовые пути – у 3 (42,9%). Одна беременность завершилась самопроизвольным выкидышем в сроке 9 недель и еще две были неразвивающимися.
Все роды срочные, в одном случае осложнившиеся частичным врастанием последа, по поводу которого выполнена гистероскопическая резекция доли плаценты диодным лазером.
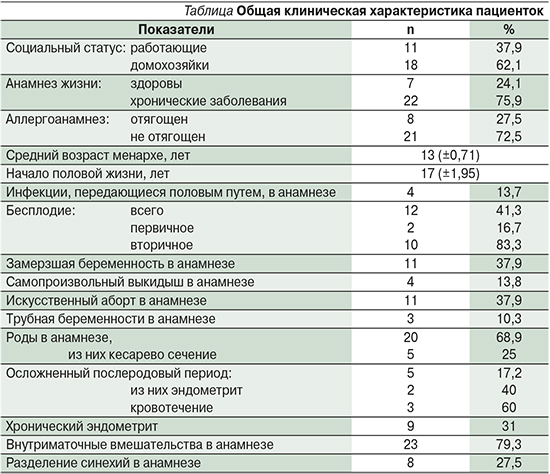
Клинический пример 1
Пациентка С. 35 лет поступила в клинику с жалобами на бесплодие в течение 2 лет, нерегуярные скудные менструации в течение года. В анамнезе: самопроизвольный выкидыш в сроке 21 неделя, инструментальная ревизия полости матки. Через 2 дня – повторное выскабливание матки по поводу остатков плацентарной ткани с развитием острого эндометрита и исходом в хронический эндометрит. В течение года – опсоменорея. Через год выполнена левосторонняя тубэктомия по поводу трубной беременности. По данным УЗИ – гипоплазия эндометрия, синехии в полости матки. При гистероскопии обширный спаечный процесс в полости матки (рис. 1). Пациентке проведены лазерный адгезиолизис, диагностическая лапароскопия с контролем проходимости маточных труб, гормональная коррекция. Контрольная гистероскопия через 2 месяца показала рецидив, выполнена оптическая диссекция единичных синехий, продолжена гормональная терапия, выполнено 2 курса внутриматочного орошения УЗ-кавитированным водным раствором 0,05%-ного хлоргексидина, 1 курс интравагинальной пелоидотерапии. Менструальный цикл восстановился после первой хирургической гистероскопии. Беременность наступила на фоне циклической гормональной терапии через 3 месяца. Срочные абдоминальные роды произошли в сроке 39 недель, родилась девочка весом 3450 г, ростом 54 см. Течение беременности и послеродового периода без особенностей.
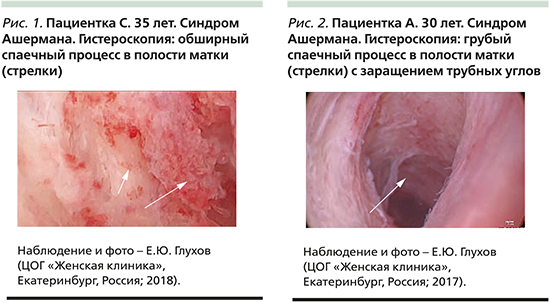
Клинический пример 2
Пациентка А. 30 лет поступила в клинику с жалобами на редкие, скудные месячные, отсутствие беременности в течение 1,5 лет. Из анамнеза: в 2016 г. – срочные самопроизвольные роды. Послеродовый период осложнился эндометритом на фоне остатков плацентарной ткани, в связи с чем произведено выскабливание стенок полости матки. Менструальный цикл восстановился через 2 месяца по типу олигоопсоменореи. По данным УЗИ – гипоплазия эндометрия (толщина М-эхо на 16-й день цикла – 5 мм), синехии в полости матки, по данным УЗ-исследования, выявлены признаки снижения овариального резерва. По данным гистероскопии, грубый спаечный процесс в полости матки (рис. 2).
В 2018 г. выполнена хирургическая гистероскопия, рассечение синехий цервикального канала и полости матки диодным лазером «Лахта Милон». Проведен полный курс реабилитации, описанный в разделе «Методы». Через 6 месяцев наступила спонтанная беременность, при доношенном сроке закончившаяся родами (мальчик, вес – 3600 г, рост – 55 см). В родах ручное обследование полости матки и отделение последа. В послеродовом периоде субинволюция матки, по данным УЗИ, остатки плацентарной ткани с признаками врастания. На 14-е сутки после родов выполнена хирургическая гистероскопия, диодным лазером удалены остатки плацентарной ткани с частичным врастанием в стенку матки.
Обсуждение результатов
Лечение и профилактика СА по сей день остаются актуальной проблемой в гинекологии. До сих пор отсутствуют доказательные данные об эффективности разработанных методов лечения этого заболевания, и, как показывают исследования, все предложенные методы, использованные в моноварианте, недостаточно эффективны.
Так, обобщенные результаты нескольких исследований, изложенные в обзоре E. Dreisler et al. [17], демонстрируют восстановление менструального цикла у 75–100% пациенток после гистероскопического адгезиолизиса, частота наступления беременности варьируется от 25 до 76%, показатель срочных родов – от 25 до 80%. Рецидивы обнаруживают в 21–42% наблюдений, и их частота зависит от степени выраженности спаечного процесса.
Гель гиалуроновой кислоты или гель полиэтиленоксид-натрий-карбоксиметилцеллюлоза для предотвращения внутриматочной адгезии были исследованы и продемонстрировали противоречивые результаты. В мета-анализе сделан вывод об отсутствии доказательств того, что гель может снижать частоту рецидивов СА после гистероскопии [18]. Однако Acunzo et al. обнаружили значительный эффект гиалуроновой кислоты по сравнению с отсутствием лечения (14 против 32% соответственно; p<0,05) [19]. Исследование, сравнивавшее внутриматочный баллон (катетер Фоллея), внутриматочную спираль (ВМС) и гель гиалуроновой кислоты, показало, что баллон и ВМС были более эффективными, чем гиалуроновая кислота [20].
Мета-анализ проспективных рандомизированных исследований показал, что пероральный прием эстрогенов не снижал риска рецидива СA [18].
С учетом вышеизложенного целесообразно рассматривать варианты комплексной терапии с использованием нескольких методов для лечения и профилактики СА. Предложенный нами вариант комплексной терапии работает сразу по нескольким направлениям. Лазерный адгезиолизис способствует меньшей травматизации эндометрия, что снижает частоту побочных явлений и осложнений, улучшает возможности иссечения спаек в труднодоступных местах. Противоспаечный барьер, введенный в послеоперационном периоде, создает искусственный временный барьер на период заживления и препятствует контакту стенок матки, образованию новых сращений между ними. Циклическая гормонотерапия эстрогенами и гестагенами, назначенная после операции, направлена на восстановление эндометрия и его циклическую трансформацию. Физиотерапия в виде орошения полости матки растворами, кавитированными низкочастотным УЗ с помощью аппарата ФОТЕК АК101, оказывает противовоспалительное, бактерицидное действия, активирует процессы регенерации эндометрия, препятствует повторному образованию синехий. Пелоидо- и магнитотерапия оказывают позитивный эффект в виде улучшения гемо- и лимфодинамики, снижают активность экссудативного и инфильтративного процессов, способствуют усилению иммунного ответа.
Непрямой сравнительный анализ результатов лечения, изложенных в публикациях последних лет, с данными, полученными в настоящем исследовании, показал следующие результаты. Hanstede et al. добились от большинства пациенток с СА восстановления полости матки с помощью гистероскопического адгезиолизиса в 1–3 попытках с частотой рецидивов 28,7% [21]; среди пациенток Bhandari et al. 63,3% потребовали повторной гистероскопии в связи с рецидивами, только у 45% – менструальный цикл стал нормальным [22]; результаты в настоящем исследовании составили 20,7 и 76,9% соответственно. В исследованиях Bhandari et al. и Yamamoto et al. после гистероскопического адгезиолизиса забеременели 26,7 и 56,3% пациенток соответственно, из них закончились родами 62,5 и 44,4% беременностей соответственно [22, 23]; частота наступления беременности среди пациенток нашего центра составила 52,6% и количество рожде-ний – 70%.
Таким образом, предложенный вариант комплексной терапии может рассматриваться как эффективный метод лечения и профилактики внутриматочных синехий.
Заключение
Комплексный подход к лечению внутриматочных синехий с применением лазерного адгезиолизиса, противоспаечного барьера, кавитированных растворов антисептика или иммумуномодулятора, интравагинальной пелоидотерапии грязями Мертвого моря и магнитотерапии позволяют улучшить результаты лечения такой сложной патологии, как СА, достичь 76,9% пациенток нормализации менструальной функции в течение 6 месяцев наблюдения и наступления беременности в течение года у 52,6% пациенток, заинтересованных в реализации репродуктивной функции, с частотой рождений 70%.
Вклад авторов. Глухов Е.Ю. – разработка концепции и дизайна исследования, сбор клинического материала, критический пересмотр первой версии статьи на предмет ее интеллектуального содержания. Дикке Г.Б. – анализ результатов статистической обработки клинического материала и их интерпретация, поиск литературных источников, написание первой версии статьи и ее редактирование после рецензирования. Нефф Е.И. – сбор клинического материала, анализ результатов, формирование иллюстративного материала для текста статьи, поиск литературных источников. Глухова В.Е., Березина Д.А. – формирование электронной базы полученных результатов, статистическая обработка данных.



